- ارتباط با ما
- |
- درباره ما
- |
- نظرسنجی
- |
- اشتراک خبری
- |
- نگارنامه
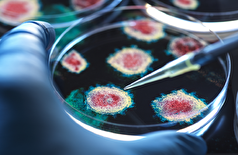
سلولهای ملانوما از استراتژی پنهانی برای زنده ماندن در درمان استفاده میکنند
به گزارش مجله خبری نگار، محققان یک استراتژی بقای پنهان را کشف کردهاند که سلولهای ملانوما برای فرار از درمان هدفمند از آن استفاده میکنند و رویکرد جدید و امیدوارکنندهای را برای بهبود نتایج درمان ارائه میدهند.
مطالعهای که در مجله Cell Systems منتشر شده و توسط محققانی از موسسه زیستشناسی سیستمها (ISB) و موسسه فناوری ماساچوست (MIT) هدایت میشود، یک مکانیسم سازگاری غیرژنتیکی و برگشتپذیر را شناسایی میکند که به سلولهای ملانوما اجازه میدهد تا پس از درمان با مهارکنندههای BRAF زنده بمانند. با شناسایی و مسدود کردن این پاسخ اولیه، محققان یک درمان ترکیبی پیشنهاد میکنند که میتواند مقاومت را به تأخیر بیندازد و اثربخشی درمانهای موجود را بهبود بخشد.
ملانوما، کشندهترین نوع سرطان پوست، اغلب در اثر جهش در ژن BRAF ایجاد میشود که رشد کنترل نشده تومور را تحریک میکند. اگرچه مهارکنندههای BRAF (مانند ومورافنیب) در ابتدا رشد تومور را متوقف میکنند، بسیاری از تومورها به سرعت با درمان سازگار میشوند و از آن جان سالم به در میبرند، که منجر به شکست درمان میشود.
برخلاف مقاومت سنتی ناشی از جهشهای ژنتیکی، این مطالعه یک فرآیند اولیه و پویای سازگاری را نشان میدهد که طی چند ساعت یا چند روز پس از درمان دارویی رخ میدهد - مدتها قبل از اینکه مقاومت ژنتیکی ایجاد شود. جالب اینجاست که این فرآیند مستقل از فعال شدن مجدد مسیر BRAF-ERK است که یک مکانیسم رایج مقاومت است.
محققان با استفاده از فسفوپروتئومیکس مبتنی بر طیفسنجی جرمی پیشرفته و تجزیه و تحلیل عمیق رونوشت، تغییرات مولکولی در سلولهای ملانوما را در طول دقیقهها، ساعتها و روزهای درمان با مهارکننده BRAF نقشهبرداری کردند.
چونمی لیو، یکی از نویسندگان این مطالعه از ISB، گفت: «ما دریافتیم که اگرچه سیگنالینگ BRAF-ERK به سرعت و به طور دائم سرکوب شد، اما سلولهای سرطانی برای بقا به فعالسازی مجدد ERK متکی نبودند. در عوض، آنها یک مسیر سیگنالینگ جایگزین، خانواده SRC کینازها (SFKs) را فعال کردند که بقای سلول و ترمیم بعدی سلول را افزایش میداد.»
کشف کلیدی در این مطالعه زمانی حاصل شد که محققان فعالسازی SFK را به گونههای فعال اکسیژن (ROS) مرتبط کردند، یک پاسخ استرس سلولی که هنگام مهار BRAF افزایش مییابد. با افزایش شدید سطح ROS، فعالیت SFK به طرز چشمگیری افزایش یافت و به سلولهای ملانوما کمک کرد تا از درمان جان سالم به در ببرند. با این حال، این سازگاری برگشتپذیر بود - پس از توقف درمان، سلولها به حالت اولیه خود بازگشتند.
با تشخیص این پاشنه آشیل، تیم تحقیقاتی یک رویکرد ترکیبی را آزمایش کرد: ترکیب مهارکنندههای BRAF با مهارکننده SFK، داساتینیب.
وی وی، یکی از نویسندگان این مطالعه از ISB، گفت: «با افزودن داساتینیب، ما این مکانیسم اجتناب تطبیقی را مسدود کردیم و به طور قابل توجهی بقای سلولهای ملانوما را کاهش دادیم و تومورها را در مدلهای حیوانی تثبیت کردیم.»
نکته مهم این است که مهار SFK به تنهایی هیچ تأثیر قابل توجهی بر سلولهای ملانوما نداشت، که این امر نیاز به درمان ترکیبی استراتژیک برای سرکوب سازگاری ملانوما قبل از ایجاد کامل مقاومت را برجسته میکند.
پروفسور جیم هیث، یکی از نویسندگان این مطالعه از ISB، گفت: «این رویکرد میتواند اثربخشی مهارکنندههای BRAF را طولانیتر کرده و نتایج بیماران را بهبود بخشد.»
این مطالعه علاوه بر آشکار کردن مکانیسم کلیدی سازگاری با دارو، اهمیت مداخله زودهنگام برای پیشگیری از آن را برجسته میکند. همچنین تجمع ROS و فعال شدن SFK را به عنوان نشانگرهای زیستی بالقوه برای شناسایی بیمارانی که ممکن است از این درمان ترکیبی بهرهمند شوند، برجسته میکند.
برای تأیید اثربخشی این استراتژی درمانی ترکیبی و تعیین پتانسیل آن برای کاربرد بالینی گستردهتر، مطالعات پیشبالینی و کارآزماییهای بالینی بیشتری مورد نیاز خواهد بود.
- لطفا از نوشتن با حروف لاتین (فینگلیش) خودداری نمایید.
- از ارسال دیدگاه های نا مرتبط با متن خبر، تکرار نظر دیگران، توهین به سایر کاربران و ارسال متن های طولانی خودداری نمایید.
- لطفا نظرات بدون بی احترامی، افترا و توهین به مسئولان، اقلیت ها، قومیت ها و ... باشد و به طور کلی مغایرتی با اصول اخلاقی و قوانین کشور نداشته باشد.
- در غیر این صورت، «نگارمگ » مطلب مورد نظر را رد یا بنا به تشخیص خود با ممیزی منتشر خواهد کرد.




- آخرین اخبار
- محبوب
- برچسب های داغ
- ۱۰ بازیکن پردرآمد جهان: رونالدو دو برابر مسی درآمد دارد و صلاح در صدر این فهرست قرار دارد
- ادعای اسپورتس ایلاستریتد، انتقال ویرتز به لیورپول بدترین انتقال تابستانی در لیگ برتر است
- علت مرگ ریکی هتون، اسطوره بوکس، مشخص شد
- بوریس جانسون اعتراف کرد که هنگام نوشتن کتاب از ChatGPT استفاده کرده است
- عکس| وزیر دفاع لیتوانی رویای ساخت دیواری شبیه به سریال «بازی تاج و تخت» در مرز روسیه را در سر میپروراند
- یک گیاه معطر ممکن است کلید کند کردن روند پیری مغز باشد
- Nature Communications: خوردن شام بعد از ساعت ۹ شب خطر سکته مغزی را افزایش میدهد
- کیم کارداشیان، ستاره سینما، رازهایی از زندگی مشترکش با همسر سابقش، کانیه وست، هنرمند مشهور، فاش کرد
- شوهر سابق بریتنی اسپیرز خبر تکان دهندهای در مورد خیانت همسرش به او فاش کرد
- چرا انار به عنوان یک نوشدارو در نظر گرفته میشود که قادر به محافظت در برابر بسیاری از بیماریها است؟
- یک مطالعه جدید، تأثیر تجاوز جنسی بر ساختار و عملکرد مغز زنان را آشکار میکند
- آیا هوش مصنوعی در شُرُف پیشی گرفتن از ذهن انسان است؟ گزارشی جنجالی پیشبینیهای هزاران متخصص را بررسی میکند
- یک هیولای انسانی که هزاران مایل از قربانیاش دور است!
- ۱۹ اتهام جداگانه علیه مربی سابق المپیک به دلیل آزار جنسی یک کودک
- مراقب جراحی زیبایی بیش از حد باشید... نتایج ممکن است نتیجهی معکوس داشته باشد!
- کیلیان امباپه دلیل نپیوستن از موناکو به رئال مادرید را فاش کرد
- از ایسلند تا کیپ ورد: با پنج کشور کمجمعیت راهیافته به جام جهانی آشنا شوید
- دانشمندان کشف کردهاند که چگونه میتوان با پنج دقیقه در روز عملکرد مغز را بهبود بخشید
- چهره درخشان تیلور سویفت... راز آن در یک روتین ساده نهفته است!
- رئیس بارسلونا فاش کرد که رابطهاش با لیونل مسی چه زمانی تیره شد
- چرا مغز زنان کندتر پیر میشود؟
- رونمایی از یک تغییر بزرگ درباره ویندوز!
- رژیم غذایی کتوژنیک مناسب برای کاهش خطر ابتلا به آلزایمر!
- اگر دچار کج شدن لب پایین هستد، بخوانید!
- کروم صفحات وب و مقالات را خلاصه سازی میکند!
- تفاله چغندر تحولی در دنیای کشاورزی!
- مایکروسافت در تلاش برای از بین بردن آلودگی هوا!
- سل در این استان ایران جولان میدهد!
- کمردرد به رده سنی جوانان رسید!
- افزایش سن مردان جهشهای مضر در اسپرم را زیاد میکند!
- ۸ عادت ساده و علمی برای حافظه معجزه میکند!
- نسخه جدید ابزار هوش مصنوعی گوگل برای ساخت ویدئو!
- چرا بوی بدن نوزادان متفاوت است؟
- کشف یک اثر عجیب بر سیاره سرخ!
- چگونه احتمال ابتلا به سرطان با مصرف گوشت را کاهش دهیم؟
- در دوران بارداری میتوان گل گاوزبان مصرف کرد؟
- ارائه مدلی متفاوت برای نظریه بیگ بنگ!
- استفاده از هوش مصنوعی کجا ممنوعیت دارد؟
- گوگل در حال ترکیب هوش مصنوعی با با گوگل مپ است!
- صبحانه چی بخوریم سالمتر است؟
- برنج پرتودهی شده چه تفاوتی با برنج ساده دارد؟
- حجم ماهوارهها و زبالههای فضایی نگران کننده میشود!
- روده شما گول نمیخورد! الگوی مصرفی غذاهای سالم را تغییر ندهید!
- درمان جدید بیماری آلزایمر روی موش موفقیت آمیز بود!
- سن سیارات منظومه شمسی چگونه تعیین میشود؟
- تحلیل رفتار فلزات با کشف جدید وارد فاز جدید شد!
- اثرگذاری ماینوکسیدیل برای درمان ریزش مو با این روش چند برابر میشود!
- چه مقدار آسپرین برای حل مشکل لخته خون پاسخگوست؟
- بستر دریاهای قطب جنوب در حال نشت گاز متان هستند!
- تبدیل گروه خونی برای پیوند کلیه!
- وضعیت ابتلا به پوکی استخوان در ایران چگونه است؟
- صحبت کردن با جنین در رحم روی آن تاثیری دارد؟
- این بیماری باعث تشدید عفونت خونی و مرگ میشود!
- تست یک واکسن آزمایشی جدید برای سرطان!
- استفاده کارمندان از ابزارهای هوش مصنوعی چه خطراتی در پی دارد؟
- کاهش خطر مرگ و میر با مصرف درست این نوشیدنی ها!
- تلاش برای ساخت دارویی که باعث رویش مجدد دندان شود!
- پرتاب نسخههای واقعی ماهوارههای اسپیسایکس چه زمانی است؟
- ۴۳ میلیون تومان هزینه برآورد شده برای رجیستری آیفون ۱۷ پرو!
- ناخنهای پا میتوانند سرطان ریه را نمایان کنند!
- چگونه عادت مسواک زدن را به کودکان بیاموزیم؟
- در ازای کاهش مصرف گوشت چه جایگزینی داشته باشیم؟
- هپاتیت A چگونه منتقل میشود؟
- ایمپلنت مغزی که میتواند دارو را به نواحی مغز برساند!
- نانوذرات به کمک درمان بیماری آلزایمر میآیند!
- سلامت تنفسی خود را با این ۵ حرکت در زمستان تضمین کنید!
- در درمان ناباروری هم جسم اهمیت دارد هم روان!
- رفع یبوست به کمک کیوی!
- سردردهای معمولی با سردردهای خطرناک چه تفاوتی دارند؟
- رژیم غذایی مدیترانهای بر پایه چه موادی استوار است؟
- جمعیت در ایران رو به پیری میرود!
- افسردگی باعث بیماریهای جسمانی هم میشود!
- میوههایی که باعث سلامت دستگاه گوارش شما میشوند!
- لوزه سوم چیست؟ چگونه میتوان آن را درمان کرد؟
- کاهش خطر زوال عقل با چند ورزش ساده!
- لایه سفید روی خیارشور نشان از خراب شدن آن دارد؟
- مصرف بیش از اندازه قند میتواند پوست را تیره کند!
- قطعهای از جنس نانو که در برابر فشار مقاوم است!
- غذاها میتوانند خاصیت درمانی داشته باشند!
- فروش رسمی رایانه هوش مصنوعی DGX Spark آغاز شد!
- کیث اربن پس از جدایی از نیکول کیدمن، رابطه عاشقانه جدیدی را آغاز کرده است: «او در شوک است.»
- مادر سلنا گومز به شایعات مربوط به رسوایی در عروسی دخترش پاسخ داد
- همسر بروس ویلیس گفت فرزندانش از همین حالا برای پدرشان سوگواری میکنند
- هواداران نیکول کیدمن پس از انتشار خبر طلاق، به کیت اربن حمله کردند
- فائزه العماری از مبارزه امباپه با شهرت میگوید
- بوفون در مورد انتخاب پسرش برای بازی در تیم ملی جمهوری چک: در ایتالیا، بار نام خانوادگیاش او را خرد میکرد
- پیشخدمت پرنسس دایانا راز جدیدی را در مورد کاخ باکینگهام فاش کرد
- پسر ۲۱ ساله راسل کرو به خاطر تصویرش مورد انتقاد قرار گرفت: «او مثل پدرش نیست.»
- نیکول کیدمن پس از جدایی از کیث اربن بیانیهای صادر کرد
- مگان مارکل به خاطر تمسخر یک مدل محکوم شد: «این حرفها خیلی گویای شخصیت واقعی اوست»
- ویکتوریا بکهام میگوید به خاطر شوهرش لبخند نمیزند
- جنیفر آنیستون اعتراف کرد که ۲۰ سال برای بچهدار شدن تلاش کرده است
- آنجلینا جولی، ستاره بینالمللی، درباره طلاقش از برد پیت، بازیگر مشهور، صحبت کرد و شکایت جدیدی علیه او مطرح کرد
- این دوچرخه سوار اسپانیایی تادژ پوگاچار را با بارسلونا یوهان کرایف مقایسه کرد
- کیت میدلتون با کت و شلوار سبز با "شکلات دبی" مقایسه شد
- جورج کلونی برای اولین بار درباره مصرف مواد مخدر صحبت کرد: «مشکلی نبود»
- شایعات نامزدی هرمیون گرنجر، ستاره هری پاتر، قوت گرفت
- «مدت زیادی تحریک و تحقیر شدم.» لروی سانه در اکتبرفست دعوا راه انداخت
- رایت: اگر کین از بایرن به تاتنهام برگردد، رکورد گلزنی شیرر در لیگ برتر را خواهد شکست
- رپر معروف، دیدی، به ۵۰ ماه زندان محکوم شد
- تام هالند برای اولین بار نامزدی خود با زندایا را تایید کرد
- نیکول کیدمن و کیث اربن جدایی خود را اعلام کردند
- حبیب پدرش را با سر الکس فرگوسن افسانهای مقایسه کرد
- مادر حدید، مدل معروف، مزرعه خانوادگیشان در پنسیلوانیا را برای فروش گذاشته است
- پسر بکهام در مورد شایعات اختلاف با والدینش: «مردم حرفهای منفی میزنند»
- ترور از GTA عشق خود را به ادبیات و داستایوفسکی اعتراف کرد
- بیول، قهرمان بوکس جهان، بدون اشاره به رونالدو، فوتبالیست ایدهآل را ترسیم کر
- هالند نروژی وقتی از او در مورد تکامل لهجهاش سوال شد، خود را بریتانیایی نامید
- جاستین بیبر اولین قدمهای پسرش را در حال پیادهروی نشان داد
- سوفیا ورگارا به دلیل بستری شدن در بیمارستان، مراسم امی را از دست داد
- شیلین وودلی پس از شش ماه رابطه عاشقانه از نامزدش جدا شد
- نیکی نیکول پس از متهم شدن به خیانت به لامین یامال، جزئیات رابطهاش با این بازیکن را فاش کرد
- بعد از مُهر رونالدو، این شماره ارزش واقعی پیدا کرد... اولین نظر از صاحب شماره «فراموش شده»!
- مشکلات زناشویی شاهزاده هری و مگان مارکل فاش شد: «به او در مورد ناتوانی جنسی هشدار داده شده بود»
- تیلور سویفت دوست داماد را به عروسی دعوت نکرد
- گواردیولا درباره برخورد ناخوشایندش با این بازیگر افسانهای در مترو صحبت کرد و گفت: «خیلی خجالت کشیدم.»
- اولین اظهار نظر دختر هالک هوگان پس از کنار گذاشته شدن از وصیتنامه پدرش
- رونی اوسالیوان، اسطوره اسنوکر، بهترین فوتبالیست، تنیسور و بوکسور تاریخ را معرفی کرد
- تیری آنری در مورد رقیب سابقش گفت: «از کاری که میتوانست بکند میترسیدم، میتوانست تو را دفن کند.»
- هافبک سمپدوریا دختری را که بیش از ۱۰ ضربه چاقو خورده بود، نجات داد
- بازیکن النصر فاش کرد که کریستیانو رونالدو چه کلماتی را به زبان عربی میداند
- «ملکه کتامین» به جرم تهیه دارویی که منجر به مرگ یکی از مشهورترین کمدینهای جهان شد، اعتراف کرد
- عکس| جورجینا پس از اعلام نامزدیاش، با حضور ویژه در کنار کریستیانو رونالدو، فالوورهایش را شگفتزده کرد
- ستاره جیمز باند برای اولین بار درباره طلاقش صحبت کرد
- وودی آلن میگوید سینماهای آنلاین را دوست ندارد
- وودی آلن، جادوگر سینمای آمریکا، داستان اشتیاق خود به هنر هفتم و باله در روسیه را روایت میکند
- جان سینا عکس مسی را منتشر کرد| این کشتیگیر ۱۰ حضور در مسابقات WWE در کارنامهاش دارد
- وین رونی: ماموران امنیتی وقتی به لبران نزدیک شدم، من را با یک هوادار اشتباه گرفتند
- خواننده ژاپنی به خاطر درخواست از مترجم برای بردنش به دستشویی محکوم شد
- بازیگر زن مشهور به دلیل افسردگی مجبور به جن گیری شد
- روما زور راز خوشبختی خانواده را فاش میکند
- سیابیتووا گفت چه نوع زنانی را نباید به همسری گرفت: "سقراط هشدار داد"
- کیتی پری در کنسرت دچار برق گرفتگی شد
- لیل پامپ، رپر آمریکایی، تصادف کرد و به خدا ایمان آورد
- زویی کراویتز به خاطر مار، حمام تیلور سویفت را بهم ریخت
- پسر بکهام در دومین عروسیاش به والدینش توهین کرد
- عکس: زلاتان ابراهیموویچ به حمزات چیمایف به خاطر کسب عنوان قهرمانی در UFC ۳۱۹ تبریک گفت
- «باید دربارهاش از او بپرسی»| نظرات خندهداری که پس از اعلام نامزدی کریستیانو رونالدو و جورجینا رودریگز به آنها داده شد
- اما استون توضیح میدهد که کدام دوره از زندگیاش را خاص میداند
- الکس فرگوسن افسانهای پاسخ داد که اگر مسی در دهه ۱۹۵۰ بازی میکرد، چه اتفاقی برایش میافتاد
- حمایت بانکها از بازار سرمایه از فردا اجرا میشود
- بورس سقوط کرده در دولت روحانی چگونه در دولت شهید رئیسی احیا شد؟
- درمان بورسی پزشکیان از زبان عبده
- جذب سرمایه ۷ همتی از بازار بورس دانشبنیانها
- وعده عناب بورسی واقعیتر شد
- چهارمین روز نزولی بازار در غیاب نیروهای صعودی
- انتخابات و دامنه نوسان مهمترین دلیل رکود فعلی بورس
- بورس با ۴ مصوبه دولت برای حمایت از بازار سهام سبزپوش میشود؟
- ۳ دلیل پایین بودن ارزش معاملات خرد در بورس
- معافیتهای مالیاتی بازار سرمایه باید استمرار پیدا کند
- بورس این روزها تحت تأثیر تداوم نرخ اخزای بالای ۳۵ درصد
- رشد شاخصهای بورس با کف سازی تکنیکال
- کاهش دامنه نوسان هم علاج بورس نزولی نبود
- سایه تامین مالی دولت بر سر بورس سنگینی میکند
- کاهش بی سابقه حجم معاملات سهام در بورسهای جهانی
- رشد شاخصهای بورس با کمک بانکیها و اعلام نرخ تسعیر ارز
- حمله به سفیر روسیه در لهستان
- معرفی سری گوشیهای Redmi K ۵۰ قبل از رونمایی رسمی
- غفوری: فکر کردن به قهرمانی از الان، سادهلوحانه است
- کاهش ۱۰ درصدی تولید هوندا در دو کارخانه
- سومین نشست دستمزد، باز هم بدون نتیجه
- لغو بلیت فروشی عمومی المپیک زمستانی چین
- گرامیداشت قربانیان هواپیمای اوکراینی در دانشگاه تورنتو
- ادامه چانهزنی چهارگانه در وین
- صرفهجویی ۱.۶ میلیارد دلاری کمیته برگزاری المپیک و پارالمپیک توکیو
- محبوبترین رشته المپیک توکیو مشخص شد
- اعلام هزینه میزبانی توکیو از المپیک و پارالمپیک ۲۰۲۰،
- آذرتاج: هیات اقتصادی جمهوری آذربایجان به ایران میرود
- بررسی عملکرد ایران در المپیک؛ جایگاه چهارمی در آسیا
- پایان وضعیت اضطراری در کشور میزبان المپیک ۲۰۲۰
- متخصصان در مورد ۵ علت احتمالی خشکی پوست هشدار میدهند
- خوردن صبحانه در اوایل صبح میتواند خطر ابتلا به بیماریهای قلبی عروقی را کاهش دهد
- نسخه فوتبال ایران را برای همیشه ببپیچیم؟
- عکس| گل نادر «گل جسد» از باغ گیاهشناسی آلمان دزدیده شد
- مهریه مجلس یا مهریه دولت؟ چکشکاری سکهها
- رابطه سمی مثل اعتیاد به مواد مخدر است؟!
- راز دوقلوهای همسان: وقتی یکی از آنها زوال عقل دارد، هر دو عمر کوتاهتری دارند
- نسخه سیاه و مبتذل روانشناسان زرد اینستاگرامی
- چگونه بمب دلاری خنثی میشود؟
- یک ادویه رایج میتواند به طور بسیار موثری با عفونتهای ویروسی مبارزه کند
- دانشمندان علت اصلی ناباروری زنان را شناسایی کردند
- هوس پروتئین: یک روند غذایی که میتواند منجر به خطرات جدی برای سلامتی شود
- خواب بسیار نامنظم با خطر بالاتر زوال عقل مرتبط است
- فقط ۱۵ دقیقه قبل از غذا خوردن میتواند شما را از سوزش سر دل و نفخ نجات دهد
- JN: آلو خشک سلامت استخوان را در زنان یائسه بهبود میبخشد
- کشف علمی، ارتباط بین عوامل مکانی و نشانگرهای بیولوژیکی پیشرفته زوال عقل را آشکار میکند
- تایمز آو ایندیا: ماهی، سویا و آجیل روند پیری مغز را کند میکنند
- یک داروی مشتق از کانابیس نتایج شگفتانگیزی در برابر تحلیل رفتن سلولهای سرطانی نشان داده است
- Frontiers in Plant Science: دانههای چیا سرشار از مواد مغذی میتوانند سلامت انسان را بهبود بخشند
- کرمهای موضعی معمولی ممکن است به سلاح جدیدی علیه سرطان تبدیل شوند
- تمرینات سادهای برای بهبود سلامت قلب نام برده شد
- گروه خونی مرتبط با بالاترین خطر ابتلا به سرطان سینه مشخص شد
- یک علت شگفتانگیز چاقی، دیابت و بیماری کبد!
- متخصصان مواد غذایی را شناسایی کردهاند که میتوانند به مدیریت استرس کمک کنند
- SMR: داروهای آرامبخش و خوابآور خطر شکستگی استخوان را افزایش میدهند
- یک کشف مهم تکاملی در مورد زندگی گوریلهای کوهستانی ماده
- Science: باکتریهای روده رشد میکروبهای بیماریزا را ۱۰۰۰ برابر کند میکنند
- نوآوری در قرنیه شفاف، راه حلی برای بحران جهانی اهدای عضو ارائه میدهد
- ترکیب جوز هندی ممکن است طول عمر را افزایش دهد
- روسیه: نوآوری جدید، لاستیکهای فرسوده را به نانولوله و هیدروژن تبدیل میکند
- قرصی به عنوان سم: دکتر میاسنیکوف درباره خطرات این پدیده هشدار میدهد
- ایالات متحده: دلفینهای مرده با ناهنجاریهای مغزی، خطر بالقوه برای انسانها را هشدار میدهند
- لنست: دانشمندان خطر تهدیدکننده زندگی ناشی از آنفولانزای فصلی را که قابل مقایسه با کووید-۱۹ است، شناسایی کردهاند
- یک آزمایش ساده اختلال نعوظ و عوارض جنسی داروهای افسردگی را پیشبینی میکند
- AJCN: شکلات تلخ اثرات مثبتی بر عملکرد شناختی دارد
- مطالعه جدید ارتباط بین رژیم غذایی و حجم مغز را نشان میدهد
- یک پزشک توضیح داد که چگونه میتوان از ابتلا به فشار خون بالا در جوانی جلوگیری کرد
- هشدار مطالعه: رسانههای اجتماعی مغز کودکان را فاسد میکنند، به ویژه به حافظه و دایره لغات آنها آسیب میرسانند
- PubMed: نمک نوآورانه فشار خون را کاهش میدهد
- ادویهها چیزی بیش از طعمدهنده هستند| فواید قابل توجه آنها را برای سلامتی و ایمنی کشف کنید
- ارز
- طلا
- بورس
- تورم
- اخبار داغ
- ورزشی
- پربیننده
- پربحث
- چین آزمایشی برای ایجاد مصنوعی بارش انجام داد
- کارشناس: با افزایش درخواستها برای انتخابات در اوکراین، زلنسکی در حال خلاص شدن از شر رقبای خود است
- یک کارشناس آمریکایی، واشنگتن را مسئول نابودی سازمانهای بینالمللی و مانعتراشی در تلاشها برای مقابله با چالشهای جهانی میداند
- آلمان قصد دارد بیش از ۷۲۰ میلیون یورو از یک بانک روسی را مصادره کند
- دانشمندان یک تهدید پنهان برای سلامتی ناشی از مواد شیمیایی موجود در بستهبندی مواد غذایی را کشف کردهاند
- روسیه و تاجیکستان در حال مذاکره برای سرمایهگذاری مشترک در میادین نفتی هستند
- پسکوف: تحویل موشکهای تاماهاک به اوکراین، تنشها را به سطح کیفی جدیدی خواهد رساند
- اوربان در اروپا روانپریشی جنگی اعلام کرد و خواستار مذاکره با روسیه شد
- دانشمندان از یک صدای وزوز غیرمعمول خبر دادهاند که زمین را فرا گرفته است
- دین هویسن نگرانیهای رئال مادرید را پیش از ال کلاسیکو افزایش داد
- اوربان آمادگی کشورش را برای میزبانی دیدار پوتین و ترامپ اعلام کرد و آن را فرصتی عالی برای صلح توصیف کرد
- ایالات متحده از افزایش علاقه کاخ سفید به تحریمها علیه روسیه خبر داده است
- دانشمندان کشف کردهاند که چگونه رواندرمانی میتواند دردهای مزمن را تسکین دهد
- مصر قصد دارد راه آهن را تا مرز غزه امتداد دهد
- پوتین از ملانیا ترامپ به خاطر مشارکتش در مسئله کودکان تشکر کرد
- اوربان از اروپا میخواهد به جای تکبر و دامن زدن به آتش جنگ، مذاکره با روسیه را آغاز کند
- دهها باکتری جدید در اتاقهای تمیز مورد استفاده برای مونتاژ کاوشگرهای فضایی کشف شدند
- محققان روسی استنت عروقی زیست تخریب پذیر را برای کاهش جراحیهای کودکان توسعه دادند
- گزارش: صنعت شیمیایی هلند پس از ترک انرژی روسیه با بحران وجودی روبهرو است
- دانشمندان به پیشرفتی در تولید سلولهای خونی دست یافتهاند
- دفتر رسانهای دولت در غزه: نوار غزه با بزرگترین فاجعه ساختمانی و انسانی در تاریخ مدرن روبهرو است
- قدیمیترین قورباغه درختی استرالیا، تکامل دوزیستان را از نو تعریف کرده است
- یک هزینه هنگفت: اروپا به دلیل رویگردانی از گاز روسیه، متحمل ضرری معادل ۱.۳ تریلیون یورو میشود
- تیم کوک، مدیرعامل اپل، قول داد که با وجود جنگ تجاری، سرمایهگذاری در چین را افزایش دهد
- دانشمندان برای اولین بار مدلهای سهبعدی از قلب گربهها را برای مقایسه با قلب انسان ایجاد کردهاند
- رسوایی در مجلس فدرال آلمان، با حضور صدراعظم مرتس
- مصر در حال آماده شدن برای راه اندازی اولین قطار پرسرعت در تاریخ خود است
- مرتس خواستار ایجاد بورس اوراق بهادار اروپا شد
- پوتین: سیستم انرژی روسیه از نظر زیستمحیطی جزو سازگارترین سیستمهای انرژی در جهان است
- وزیر امور خارجه مراکش: روسیه شریکی قابل اعتماد و بازیگری مهم در صحنه بینالمللی است
- لوپن از بودجه ۲۰۲۶ فرانسه انتقاد کرد
- یک کارمند سابق پنتاگون مدعی شد که موجودات فضایی هزاران سال است که در زمین حضور دارند
- فیفا به تهدیدهای ترامپ در مورد انتقال مسابقات جام جهانی ۲۰۲۶ پاسخ داد
- یک پیشرفت پزشکی جدید، جهان را به پیوند کلیههای سازگار با همه گروههای خونی نزدیکتر میکند
- پوتین: روسیه حدود ۱۰ درصد از تولید نفت جهان را تامین میکند
- وزیر دفاع سوئد راهی برای ترغیب روسیه به صلح ارائه کرده است
- دانشمندان هشدار میدهند که آلودگی هوا خطر ابتلا به صرع را افزایش میدهد
- اتحادیه اروپا در حال آماده شدن برای ارائه کمک مالی به مصر است
- وزارت امور خارجه چین: درخواست ترامپ برای کنار گذاشتن نفت روسیه، به عرضه جهانی نفت آسیب میرساند
- ترامپ تصمیم گرفته است در تعداد یخشکنها با پوتین رقابت کند
- رسانههای غربی: اروپا به دلیل اوکراین در هرج و مرج فرو خواهد رفت
- ستاره شناسان معمای «گلولههای گازی» سیاهچالههای عظیم را حل کردند
- یک غافلگیری بزرگ: یک ژنرال آمریکایی هدف بالقوه موشکهای تاماهاک را فاش میکند
- روسیه روشی برای افزایش اثربخشی درمان سرطان با استفاده از طلا ابداع کرده است
- وزیر انرژی ترکیه: دیدار با مدیرعامل شرکت گازپروم روسیه مفید بود
- هیئت روسی در وین: تلاشها برای «لغو» روسیه منجر به مشکلاتی در کشورهای غربی شده است
- گفته شد که چرا مردان باروری خود را از دست میدهند
- دانشمندان هشدار میدهند که احیای کره زمین پس از گرمایش جهانی صدها هزار سال طول خواهد کشید
- مادورو کودتاهای سیا در آمریکای لاتین را محکوم کرد
- ایالات متحده مشخص کرد که چرا کشتی تایتان با میلیاردرها در آن غرق شد
- دانشمندان یک الگوریتم جهانی برای رفتار حیوانات کشف کردهاند
- باستان شناسان "دنیای گمشده" اجداد انسان را در سواحل جاوه کشف کردند
- ۳۶ نفر در موریتانی بر اثر دیفتری و تب دره ریفت جان باختند
- اتحادیه اروپا میخواهد سیگارهای فیلتردار را ممنوع کند
- شایعترین آسیبها در بین اسکوترسواران شناسایی شده است
- اوربان: مجارستان در صورت آسیب دیدن شرکتهای فعال ما در روسیه، از مصادره داراییهای روسیه حمایت نخواهد کرد
- رئیس جمهور کلمبیا دستور انتقال طلای مصادره شده به غزه را صادر کرد و پیشنهاد تشکیل یک ارتش بین المللی برای بازسازی نوار غزه را داد
- ترامپ در مورد از دست دادن جایزه نوبل به شوخی گفت: «سال آینده بهتر خواهد بود»
- یک پزشک توضیح داد که چرا نباید چای را با گندم سیاه بنوشید
- مدیر عامل صندوق بینالمللی پول قصد دارد برای حمایت از جاهطلبیهای این صندوق برای بسته وام جدید، به کییف سفر کند
- ترامپ: من سخت تلاش میکنم تا به درگیریها در اوکراین پایان دهم
- سرمای شدید جنوب سیبری و خاور دور را فرا گرفت
- افشاگری تکان دهنده: اعتیاد به پورن باعث شد پدری در آریزونا عمداً دختر دو ساله خود را به قتل برساند
- ترامپ قول داد که در مورد درخواستهای اوکراین برای سلاحهای دوربرد تصمیم بگیرد
- ترامپ قصد دارد در حاشیه اجلاس آسهآن با مودی دیدار کند
- اولین اظهار نظر امیر قطر پس از پیروزی کشورش مقابل امارات و راهیابی به جام جهانی
- لاوروف اظهار داشت که «افراد» ناتو «بسیار فعالانه لاف میزنند»
- بیماریهایی که میتوانند از التهاب لثه ناشی شوند، شناسایی شدهاند
- بلاروسوف: روابط بین روسیه و بلاروس الگویی برای مقابله با جنگ هیبریدی است که غرب به راه انداخته است
- سنای آمریکا آماده است تا به ترامپ اختیار اعمال تعرفههای گمرکی تا سقف ۵۰۰ درصد علیه چین را بدهد
- پزشکان برای اولین بار پیوند مثانه را روی انسان انجام دادند
- ویلی سانیول، سرمربی گرجستان: اسپانیا انگار از سیاره دیگری آمده اس
- وزیر انرژی عربستان سعودی در مسکو: امنیت انرژی مسیر رفاه است
- نروژ میلیاردها یورو برای حمایت از اوکراین در سال ۲۰۲۶ اختصاص خواهد داد
- یک عامل غیرمنتظره که مانع رشد شغلی میشود، شناسایی شده است
- اولین واکنش پاری سن ژرمن در مورد جذب لامین یامال
- کمیته حمایت از روزنامهنگاران: اسرائیل مسئول ۹۵ درصد از قتل روزنامهنگاران در خاورمیانه از ۷ اکتبر تاکنون است
- وزیر دفاع بلاروس: اتحادیه اروپا در حال ایجاد یک بخش هستهای مستقل از آمریکا و ناتو است
- مصر و امارات متحده عربی توافقنامهای برای تامین برق اروپا امضا کردند
- تهران: توافق با مسکو برای ساخت هشت راکتور هستهای جدید در ایران
- مذاکره المپیک لیون با هانس هاتبور!
- گام تعیینکننده اثر کنان ییلدیز
- یک شاختار دونتسک دیگر در روسیه بازی خواهد کرد
- موضع رودیگر در مورد آیندهاش در رئال مادرید مشخص شد
- آنچلوتی از حجم صحبتها در مورد سرنوشت نیمار در تیم ملی برزیل نگران بود
- تیم ملی فوتبال آفریقای جنوبی برای اولین بار از سال ۲۰۱۰ در جام جهانی فوتبال شرکت خواهد کرد
- سیمئونه تصمیم گرفته است: اتلتیکو مادرید نگاهش را به کلوب بروژ دوخته است
- لروی سانه ناامیدکننده ظاهر شد
- اولین تماسها برای جذب بردلی بارکولا
- گلادیلین درباره پدرو در الاهلی: اگر او میخواهد پول دربیاورد، دلیلی برای نگه داشتنش وجود ندارد
- منچستریونایتد آماده است ۷۸ میلیون پوند برای ستاره یوونتوس بپردازد
- باشگاه موناکو درباره آینده فاتی که به صورت قرضی از بارسلونا به این تیم پیوسته صحبت کرده است
- برایان گیل دوباره خودش را تایید کرد
- باشگاه فوتبال بارسلونا جستجوی خود برای یک مهاجم را در ایتالیا به طور دقیق تنظیم میکند!
- ناصر الخلیفی آتش جنگ رئال مادرید و بارسلونا را شعلهور کرد
- آینتراخت فرانکفورت میخواهد تیم خود را با مهاجم نیوکاسل یونایتد، تاولیری، تقویت کند
- اولیویرا: زنیت برای نینو ۱۵ تا ۱۸ میلیون یورو از کروزیرو درخواست کرد، اما باشگاه از قیمت پیشنهادی منصرف شد
- اتلتیک: رئال مادرید معتقد است کارواخال و ترنت میتوانند برای ال کلاسیکو ریکاوری کنند
- مسی ۱۰ استعداد جوان خود را معرفی کرد... بدون لامین یامال
- آیندهای برای روبرت لواندوفسکی در اسپانیا: نه بارسلونا
- هانس هاتبوئر، قراردادش بسته شد
- کین رکورددار گلزنی برای تیم ملی انگلیس از یک باشگاه غیرانگلیسی است
- تمام تیمهای آفریقایی که مستقیماً به جام جهانی ۲۰۲۶ راه یافتهاند، اعلام شدند
- گراهام پاتر، سرمربی سابق چلسی، آماده هدایت تیم ملی سوئد است
- بازگشت فرانک کسیه از همین حالا در دست بررسی است
- ویلیان پاچو در آستانه امضای قرارداد
- رقیب جدید بسیار بزرگ برای جذب دایوت اوپامکانو
- سرمربی اسپانیا، د لا فوئنته: پدری بازیکن واقعاً شگفتانگیزی است
- استونینکو: تیم ملی ایتالیا با مسابقات پلیآف مقدماتی جام جهانی و افکار ناخوشایندی روبهرو است
- ماتیاس آلمیدا خواهان یک قهرمان ایتالیایی برای خط حمله است
- حمله پاری سن ژرمن به خرید ۶۰ میلیون دلاری نیوکاسل
- میکل مرینو پدال گاز را رها نمیکند
- جردن پیکفورد، دروازهبان تیم ملی انگلیس، بیش از یک سال است که گلی دریافت نکرده است
- مسی یک تورنمنت فوتبال جوانان ایجاد کرده است که بارسلونا، چلسی و منچستر سیتی در آن شرکت خواهند کرد
- گاردین فهرستی از ۶۰ بازیکن آیندهدار تهیه کرده است که شامل سه نماینده از کشورهای مستقل مشترکالمنافع میشود
- ماده مهر و موم شده توسط رولاندو ماندراگورا
- تصمیمی سرنوشتساز برای کارلوس بالبای مورد نظر
- سائول ایگز میخواهد به اتلتیکو مادرید بازگردد
- ایلیچیچ درباره آتالانتا: میتوانستیم با چشمان بسته بازی کنیم و باز هم گل بزنیم
- دمبله پس از قهرمانی در لیگ قهرمانان اروپا، در حال مذاکره با پاری سن ژرمن برای تمدید قراردادش است
- ایلیچیچ در مورد آتالانتا در فصل ۲۰۱۹/۲۰۲۰ گفت: «ما میتوانستیم به فینال لیگ قهرمانان اروپا برسیم.»
- مارتین زوبیمندی، رهبر ارکستر
- پیشنهاد بزرگی که رافینیا را مردد کرد
- آینده مبهم آنتونیو رودیگر
- رافینیا، وینگر بارسلونا، توضیح میدهد که چرا به یک باشگاه عربستانی نپیوسته است
- تباس و لاپورتا برای برگزاری مسابقه در آمریکا، بازیکنان را نادیده گرفتند
- زنیت قصد دارد برای مهاجم ۱۹ ساله پالمیراس ۱۵ میلیون یورو پیشنهاد دهد
- ویکتور فرودولت علاقه اتلتیکو مادرید را رد کرد
- نبرد آشکار برای گیلبرتو مورا
- باشگاه موناکو خواستار آرامش در مورد آنسو فاتی شد
- سیسه در مورد اکیتیِک: انتظار نداشتم اینقدر خوب و سریع باشد
- کواچ در مورد بازی پیش رو بوندس لیگا: بایرن شانس بیشتری برای برد دارد
- کمپانی در مورد بازی پیش رو مقابل بروسیا: این یک بازی کلاسیک است. احساسات اینجا نقش بزرگی ایفا میکنند
- وینیسیوس جونیور حتی با ۲۲۵ میلیون یورو هم رئال مادرید را ترک نخواهد کرد
- تصمیم برکناری پاونوویچ تصمیم من بود
- جوب بلینگهام، خرید غیرمنتظره برای ژانویه
- هری کین: حس میکنم بایرن خانه دوم من است
- سیسه درباره شانس قهرمانی مارسی: باید در این فصل خوشبین باشیم
- جنارو گتوزو، سرمربی تیم ملی ایتالیا، اعلام کرد که در صورت عدم راهیابی تیم ملی این کشور به جام جهانی ۲۰۲۶، از این تیم جدا خواهد شد
- ژان فیلیپ متتا در حال پیشرفت است
- تغییر اساسی در برنامه جذب گوئهی
- فدریکو دیمارکو، وسوسه لیگ برتر
- موندو دپورتیوو: وینیسیوس به دلیل برهم زدن آرامش در دادگاه حاضر خواهد شد
- سیسه درباره عملکرد لیورپول: گاهی اوقات اوضاع بد پیش میرود، اما باید مثبت اندیش ماند
- کاسمیرو در مورد شکست برزیل مقابل ژاپن گفت: «بگذارید این یک درس عبرت باشد.»
- عثمان دمبله خواستههای میلیون دلاری برای امضا دارد
- دو قهرمان اروپا، با توجه به برونو فرناندز
- واقعیت اقتصادی جدید اینتر میلان
- سولباکن، سرمربی نروژ: باب مقابل نیوزیلند وحشتناک بازی کرد
- روی کین درباره رشفورد: او برای اطرافیانش مشکلساز شده است
- رئیس باشگاه مارسی در مورد تصمیم برای جذب گرینوود: زمان همه چیز را مشخص خواهد کرد
- زنگهای خداحافظی برای تکهای از آینتراخت فرانکفورت
- آردا گولر صحبتهایش را آغاز میکند
- دوئل چهارجانبه برای خفرن تورام
- استونز در مورد صعود انگلیس به جام جهانی ۲۰۲۶: باورنکردنی است که توخل چگونه همه چیز را در چنین مدت کوتاهی کنار هم قرار داده است
- پایشاو درباره مارسی: در هر بازی احساس خوبی دارم و اعتماد به نفس دارم
- اینتر میلان به جذب مارک گوئهی علاقهمند است
- تغییر اساسی در برنامه جذب گوئهی
- بارسلونا به دنبال جذب کنان ییلدیز است!
- اریک گارسیا ترجیح خود را به روشنی بیان میکند