- ارتباط با ما
- |
- درباره ما
- |
- نظرسنجی
- |
- اشتراک خبری
- |
- نگارنامه
بهبود فیبروز کبدی با ابداع روش درمانی جدید
به گزارش مجله خبری نگار/تکناک: استفاده از این روش، یک روش درمانی جایگزین امیدوارکننده برای داروهای سنتی است.
بزرگترین چالش در توسعه یک درمان موفق RNA، تحویل هدفمند آن است. تحقیقات در حال حاضر با محدودیتهای فعلی LNPs مواجه است که بسیاری از بیماریها را بدون درمان موثر RNA رها کرده است.
فیبروز کبد زمانی رخ میدهد که کبد به طور مکرر آسیب ببیند و روند بهبودی منجر به تجمع بافت اسکار شود و عملکرد سالم کبد را مختل کند. این بیماری یک بیماری مزمن است که با تجمع بیش از حد ماتریکس خارج سلولی غنی از کلاژن (ECM) مشخص میشود. درمان فیبروز کبدی با استفاده از درمانهای RNA به دلیل فقدان سیستمهای تحویل برای هدف قرار دادن فیبروبلاستهای فعال ساکن کبد، همچنان چالش برانگیز است. هم ساختار فیبروبلاست جامد و هم فقدان ویژگی یا میل ترکیبی برای هدف قرار دادن این فیبروبلاستها، مانع از ورود LNPهای فعلی به فیبروبلاستهای فعال ساکن کبد شده بنابراین آنها قادر به ارائه درمانهای RNA نیستند.
مایکل میچل، جی پیتر و گری اسکیرکانیچ، و همکاران شان در این تحقیق، زوکسیانگ هان و نینگ کیانگ گونگ، متوجه شدند که برای مقابله با این موضوع و کمک به ارائه درمان برای میلیونها نفری که از این بیماری مزمن رنج میبرند، بایدروشی جدید برای سنتز LNPهای متصل به لیگاند، افزایش گزینش پذیری آنها و امکان هدف قرار دادن فیبروبلاستهای کبدی پیدا کنند.
مطالعه آنها که در مجله Nature Communications منتشر شده است، نشان میدهد که چگونه یک لیگاند (ماده شیمیایی) مولکولی کوچک میل به فیبروبلاستهای فعال شده در کبد را ایجاد میکند و به سختی ساخت کلاژن را هدف قرار میدهد.
تجمع کلاژن با افزایش آزادسازی پروتئین شوک حرارتی ۴۷ (HSP۴۷) همراه است که پروتئینی است که بیوژنس (زیست زایی) و ترشح کلاژن را هدایت میکند. آزادسازی بیش از حد پروتئین HSP۴۷ و افزایش بیوژنز کلاژن، در نهایت به فیبروز تبدیل میشود.
هنگامی که LNPهای آنها به سلول هدف رسیدند و وارد آن شدند، siRNA آزاد میشود تا HSP۴۷ را خاموش کند، تولید کلاژن را مهار کند و فیبروز را در مسیرهای آن متوقف سازد. این درمان که در موشها موفقیت آمیز نشان داده شده است، یک درمان RNA امیدوارکننده برای فیبروز کبدی در انسان است.
این رویکرد جدید برای سنتز لیپیدهای قابل یونیزاسیون، کلید باز کردن درهای بیشتری برای کاربردهای درمانی RNA برای درمان بیماریهای مختلف است.
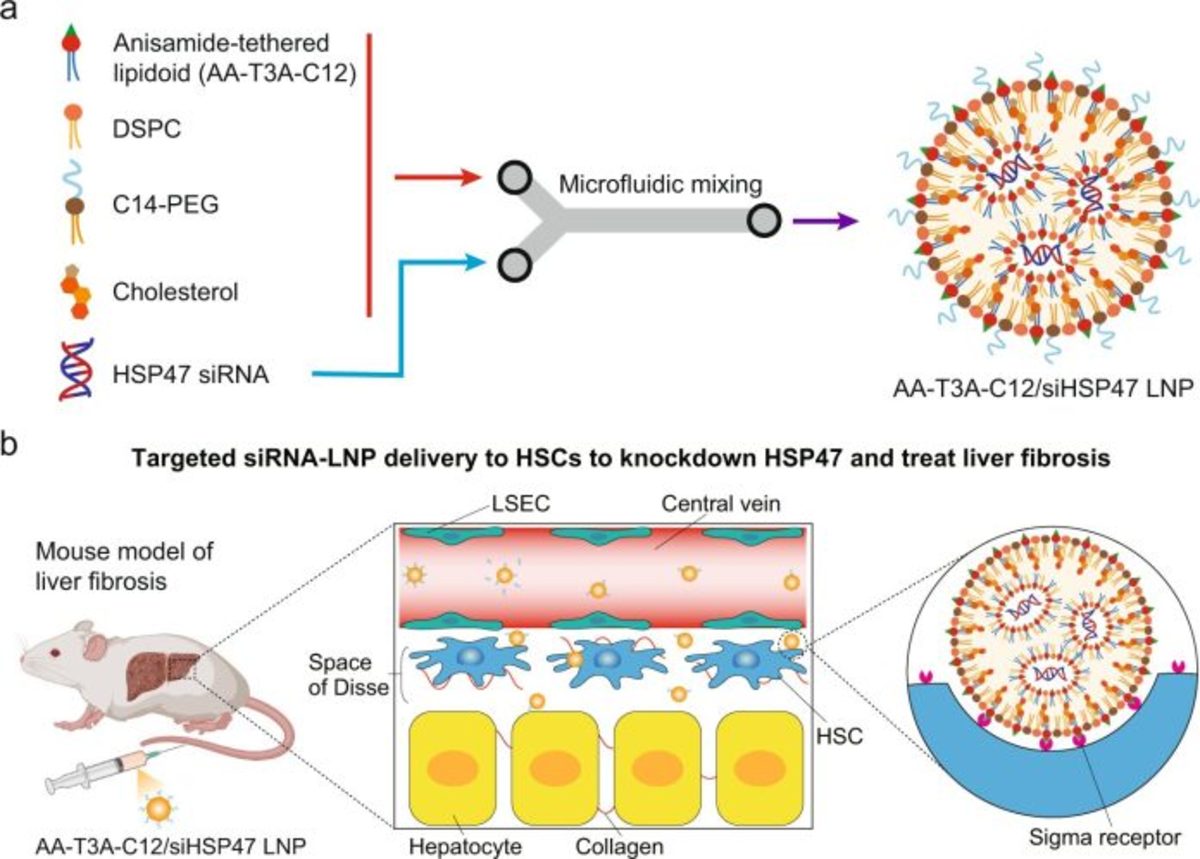
دکتر میچل گفت: برای اینکه LNPهایی به اندازه کافی مناسب را برای هدف قرار دادن سلولهای ستارهای کبدی یعنی آنهایی که فیبروز را تحریک میکنند، انتخاب کنیم، یک لیگاند آنیسامید که مولکولی است که میل ترکیبی بالایی با گیرنده روی این سلولهای ستارهای دارد، در ساختار لیپید یونیزاسیون پذیر وارد کردیم. اساسا، ما یک مکانیسم قفل و کلید را برای هدف قرار دادن و باز کردن تحویل به این سلولهای غیرقابل دسترسی ایجاد کردیم.
فرآیند سنتز توسط هان و همکارانش به عنوان یک فرآیند “یک در دو مرحله ای” توسعه داده شد. برای ایجاد مجموعهای از لیپیدهای قابل یونیزاسیون، تیم تحقیقاتی ابتدا یک پیش ساز لیگاند آنیسامید (AA) و هستههای آمینه مختلف را کنار هم قرار دادند. آنها سپس دمی آبگریز را برای ایجاد لیپیدهای یونیزاسیون AA اضافه کردند. انیسامید به دلیل ماهیت خنثی و پایدار و همچنین تمایل آن به گیرندههای سیگما بیش از حد در سلولهای ستارهای، به عنوان لیگاند انتخاب شد. هنگامی که مجموعه LNPهای متصل به AA ایجاد شد، تیم تحقیقاتی توانایی آنها را برای هدف قرار دادن و ارائه درمان به سلولها از طریق یک فرآیند انتخاب، دو دور تجزیه و تحلیل کرد.
هان گفت: ما نیاز داشتیم یک LNP خاص متصل به AA پیدا کنیم که هم قوی و هم مناسب باشد. دور اول فرآیند انتخاب با بررسی اینکه LNPهای ما چقدر میتوانند پروتئین فلورسانس سبز (GFP) را در فیبروبلاستها برای اندازه گیری قدرت از بین ببرند، انجام شد. GFP شواهد بصری بسیار خوبی را برای اینکه چگونه RNA درمانی، آزادسازی ژن را در زمان واقعی خاموش میکند ارائه میدهد.
وی ادامه داد: در دور دوم، ما توانایی انتخابی این LNP قدرتمند را آزمایش کردیم. ما این کار را با مسدود کردن گیرنده سیگما انجام دادیم تا بفهمیم که گروه لیگاند AA خاص چقدر در توانایی LNPها برای ورود به سلولهای هدف مهم است. در حقیقت ما نشان دادیم که گروه AA قابل توجه است؛ پس از محاصره گیرنده سیگما، قفل و کلید را از دست دادیم و دیدیم که LNP متصل به AA وارد سلول هدف نمیشوند.
این تیم AA-T۳A-C۱۲ را به عنوان یک siRNA درمانی قوی و انتخابی حامل LNP شناسایی کردند که قادر به کاهش ۶۵ درصدی آزادسازی HSP۴۷ در موشها و همچنین بهبود بافت آسیب دیده کبد است. نتایج این مطالعه نشان میدهد که AA-T۳A-C۱۲ LNP از MC۳ LNP که یک ناقل غیر ویروسی است که برای درمانهای بالینی استفاده میشود و برای استفاده در درمان RNA سلولی فیبروز کبدی مورد تایید FDA قرار گرفته است، بهتر عمل میکند.
این LNP جدید متصل به لیگاند، نوعی درمان RNA برای فیبروز کبدی ارائه میکند و به وسیلهی سنتز راهی برای تطبیق LNPها با سایر سلولها و بافتهای بدن که قبلاً هدفشان سخت بود، فراهم میکند.
هان میگوید: پتانسیل LNPها بسیار زیاد است، ما LNPها را هوشمندتر و کارآمدتر میکنیم.
میچل افزود: ما هیجان زده ایم که یک درمان عالی پیدا کرده ایم که ریشه ژنتیکی این بیماری کبدی را برطرف میکند؛ و از آنجایی که این وسیله انتقال LNP، در سلولهای فیبروتیک کبد کار میکند، ممکن است منجر به ایجاد درمانی برای انواع دیگر فیبروز در بدن شود، مانند فیبروزی که در ریه یا تومورها ایجاد میشود.
وی در ادامه گفت: فراتر از آنچه در کبد بررسی کرده ایم، این روش ایجاد LNP میتواند برای درمان انواع سلولهای دیگر استفاده شود. ما به طور بالقوه میتوانیم سلولهای مغز، ریهها یا قلب را با نصب لیگاندهای هدفگیری خاص در ساختار لیپیدی قابل یونیزاسیون هدف قرار دهیم. راههای زیادی در اینجا وجود دارد و ما هیجان زده هستیم که این تحقیقات را در جهتهای جدیدی ادامه دهیم.
- لطفا از نوشتن با حروف لاتین (فینگلیش) خودداری نمایید.
- از ارسال دیدگاه های نا مرتبط با متن خبر، تکرار نظر دیگران، توهین به سایر کاربران و ارسال متن های طولانی خودداری نمایید.
- لطفا نظرات بدون بی احترامی، افترا و توهین به مسئولان، اقلیت ها، قومیت ها و ... باشد و به طور کلی مغایرتی با اصول اخلاقی و قوانین کشور نداشته باشد.
- در غیر این صورت، «نگارمگ » مطلب مورد نظر را رد یا بنا به تشخیص خود با ممیزی منتشر خواهد کرد.
- آخرین اخبار
- محبوب
- برچسب های داغ
- عواقب خطرناک طلاق برای مردان ذکر شد
- در شصت سالگی، او بهطور اتفاقی کشف کرد که پدرش یک «جنایتکار جنگی» است
- استرس باعث پرخوری میشود؟ علم دلیل پنهان افزایش اشتها را آشکار میکند
- اثر غیرمنتظره کافئین بر عملکرد آنتیبیوتیکها
- ژاپن چهلمین رکورد امید به زندگی زنان را ثبت کرد
- فیلم| محمد صلاح هواداران منچستر یونایتد را به خاطر پیراهنش عصبانی کرد
- ویدئو| یک جواهرساز مشهور به رونالدو یک ساعت لوکس ساخته شده از یاقوت کبود شفاف هدیه داد
- ۳ حقیقت شگفتانگیز درباره بوی بدن و چگونگی حفظ شادابی در تمام طول روز
- عکس| یک شگفتی ۷۸۰۰۰ ساله: ردپاها تاریخ نئاندرتالها را از نو مینویسند
- یک اشتباه آشکار در خوردن موز نامگذاری شده است
- توضیح علمی برای ظاهر شدن چین و چروک با افزایش سن
- دانشمندان پرم دریافتند که ترس و طمع چگونه بر نرخ بیت کوین تأثیر میگذارد
- مدت زمان ادرار سالم نامگذاری شده است
- ۴ گروه غذایی مفید برای درد مفاصل
- کشوری که قدرتمندترین گذرنامه جهان را دارد، معرفی شد
- دانشمندان کشف کردهاند که چرا همه موجودات زنده طبق یک اصل مشابه میخوابند
- داستانهای علمی تخیلی به واقعیت نزدیکتر میشوند| مبارزه با سوسکها تحت کنترل انسان!
- عکس| مدل موی بد دیوید بکهام باعث خنده همسرش شد
- بدون جایگزین کردن شیر یا حذف شکر| ۵ راه برای سالمتر کردن قهوه صبحگاهیتان
- برند معروف پیتزا: «آیا ایساک به یونایتد میپیوندد یا با یک باشگاه بزرگ قرارداد امضا میکند؟»
- جزئیات آزمایش نخستین داروی لاغری جهان!
- حقایقی جالب در مورد دومین غول گازی منظومه شمسی!
- وقتی نخ دندان جایگزین سوزن میشود!
- علائم سکته گرمایی که باید بدانید!
- مسیر تکراری یا خاطره تکراری در مغز بازسازی نمیشود!
- هلو برای کاهش وزن به شما کمک میکند!
- با بهترین زمان خواب شبانه آشنا شوید!
- معرفی چشماندازی از آینده تعامل انسان و کامپیوتر!
- استفاده نوجوانان از هوش مصنوعی به این شکل عجیب!
- بزرگترین تحول اقتصادی در دستان هوش مصنوعی!
- دو موردی که میتواند پیشرفت دیابت را کُند کند!
- دو روش ساده و سریع برای کاهش فشار روانی!
- منظومه شمسی چگونه به پایان میرسد؟
- روایت تکامل خزندگان چیزی نیست که تصور میکردیم!
- مفهومی تازه در دنیای فناوری! تفکر بومی مبتنی بر هوش مصنوعی!
- فناوری نانوحباب خطرات ترکیبات آلی خطرناک را حذف میکند!
- آمیگدال برای دور زدن نواحی مغزی تکامل پیدا کرد!
- قحطی اینترنت ماهوارهای استارلینک فاجعه آفرین شد!
- واتساپ با آزمایشی تازه به بازار برمیگردد!
- چت جیپیتی نمیتواند پزشک باشد!
- ریفلاکس چند درصد ایرانیان را درگیر کرده است؟
- زباله ژنتیکی فرمانهای اصلی تنظیم ژنهای انسانی را صادر میکنند!
- رونمایی از قابلیتهای جدید هوش مصنوعی در «گوگل فوتوز»!
- کبد چگونه بیمار میشود؟ + راههای پیشگیری!
- کیک و بیسکوئیت و آبمیوه برای کودکان صبحانه نمیشود!
- راز تعاملات پنهان میان نوترینوها کشف شد!
- برای دفع سنگ کلیه خربزه بخورید!
- در تابستان ضدیخ کاربرد دارد؟
- نوشیدنی در فضای باز فاسد میشود؟
- یک گروه خونی خاص افراد را در معرض سرطان سینه قرار میدهد!
- از شایعترین مشکلات گوارشی اربعین چگونه پیشگیری کنیم؟
- پیشگویی از آینده واقعیت دارد یا یک توهم است؟
- ساخت تراشهای که میدانهایی با قدرت بالا تولید میکند!
- کشف سیارهای جدید و اسرارآمیز با ویژگیهای جالب!
- فرایند توسعه اپلیکیشنهای هوشمند با معرفی Spark تسریع شد!
- برای اولین بار حرکت اتمها با وضوح بالا ثبت شد!
- کشف رازهای جدیدی درباره اجرام فرانپتونی!
- جاسوسی به اسم استارلینک!
- با قرص میتوان حافظه را تقویت کرد؟
- گرگرفتگی چه مدت طول میکشد؟ چرا اتفاق میافتد؟
- حذف صبحانه منجر به کاهش تمرکز میشود!
- راهکارهای طب سنتی برای پیشگیری از زوال عقل!
- رایحهدرمانی میتواند سطح اضطراب را کاهش دهد!
- بهبود عملکرد معده و کاهش نفخ با ترکیب شربت گلاب-بهلیمو!
- مصرف میوههای تازه سیستم ایمنی بدن شما را تقویت میکند!
- رباتی که برای اولین بار عمل قلب انجام داد!
- محصولات پروبیوتیک کمک کننده برای بهبود سلامت گوارش شما!
- کاهش مصرف میزان سیگار و قلیان در جوانان!
- آمار مصرف فستفودها در بین کودکان کاهش یافت!
- چه کنیم تا از عفونتهای گوارشی فصل گرما در امان بمانیم؟
- نوشیدنیهای انرژیزا خطری برای آسیب به کبد!
- کمبود ویتامین D چه تاثیرات منفی بر سلامتی دارد؟
- آنتیبیوتیکها بیماریهای ساده را به چالشی مرگبار تبدیل میکنند!
- اصلاح عادات روزمره شما را از شر بیماریها نجات میدهد!
- مشکلات خواب چه عوارضی برای سالمندان دارد؟
- نرخ ابتلا به دیابت نوع ۲ در جوانان در حال افزایش است!
- روغن زیتون شدت حملات میگرنی را کم میکند!
- بیماریهای مزمن با الگوی درست خواب کاهش پیدا میکنند!
- مصرف این مقدار آب سنگ کلیه را از شما دور میکند!
- سرعت شارژ گوشیهای آیفون تا ۶۶ درصد بهبود بخشیده شد!
- کارگردان، وینونا رایدر را گیر انداخت و تهدید کرد که حرفهاش را خراب خواهد کرد
- جنیفر لوپز در تولد ۵۶ سالگیاش عکسی از دوران کودکیاش به همراه کیک منتشر کرد
- رسوایی جنسی جدیدی گریبان مائورو ایکاردی را گرفته است
- شوچنکو، اسطوره تیم ملی اوکراین، با قهرمان مطلق بوکس جهان، اوسیک، دیدار کرد
- حادثه تکان دهنده: مبارز MMA در دعوا با دختر، یک چشم خود را از دست داد
- «با کت و شلوار سفید. ۲۳ سال پیش...» ریو فردیناند در مورد امضای قرارداد با منچستر یونایتد
- هالند عکسی از تعطیلاتش را برای جشن تولدش منتشر کرد: «در نیمه راه ۵۰ سالگی!»
- قهرمان جهان روسیه درباره افسردگی پس از زایمان صحبت میکند
- راموس به واسکز که پس از ۱۰ سال رئال مادرید را ترک کرد، گفت: «به زودی میبینمت»
- انس جابر برای «کشف دوباره شادی زندگی»، بازنشستگی خود را از تنیس اعلام کرد
- La Nacion: الکسیس سانچز با مدل روسی رابطه برقرار کرد
- مسی جزئیات درگیری با رابرت لواندوفسکی در سال ۲۰۲۱ را فاش کرد
- سوفی ترنر رابطهاش را با نامزد سابقش از سر میگیرد
- النا دودینا درباره بارداری در ۳۶ سالگی: «شرمآور بود که هیچکس متوجه نشد»
- جنیفر آنیستون مظنون به داشتن رابطه جدید با یک هیپنوتراپیست است
- کایلی جنر به همراه تیموتی شالامی در تعطیلات در ایتالیا دیده شدند
- عکس| گروه اوئیسیز در اولین کنسرت خود پس از ۱۶ سال، به دیوگو ژوتا ادای احترام کردند
- دختر ۱۱ ساله تیماتی میخواهد مادر جوانی شود
- پس از یک "خیانت احتمالی"، نامزد فرمین لوپز، ستاره بارسلونا، عکسی از خودشان با هم منتشر کرد
- تیلور سویفت با پیراهنی به ارزش ۴۰۰۰ روبل در ملاء عام ظاهر شد
- عکس| واکنش پدی پیمبلت، مبارز UFC، به مرگ فوتبالیست دیوگو ژوتا
- زارع: ما زیر بار زور و تسلیم نمیرویم
- گلر مس رفسنجان: جنگ تمام میشود، اما وطن فروشها فراموش نمیشوند
- «من بیدفاع رها شده بودم»: بدلکار از کوین کاستنر شکایت کرد
- در دو کلمه| کریستیانو رونالدو باشگاه مادرش را غافلگیر کرد + عکس
- الکساندر اووچکین به افتخار رکورد اسنایپر NHL از دیوید بکهام هدیه دریافت کرد
- فصل جدید: شهادتهای غافلگیرکننده در پرونده مرگ مارادونا
- این بازیگر با فرزندان زیاد گفت که چگونه پس از ۴۵ سال فرم خود را حفظ میکند
- امیلی اوسمنت پس از کمتر از ۵ ماه از ازدواج درخواست طلاق میکند
- شهادت جدید جزئیات جدی در مورد روزهای پایانی مارادونا را فاش میکند
- شاهزاده هری و مگان مارکل بیانیهای غافلگیرکننده در مورد بریتانیا بیان کردند
- یک هنرمند مصری حقیقت ازدواج خود با محمد صلاح را فاش میکند
- "من خنده دار به نظر میرسم": خواننده رپ معروف به دلیل فلج صورت در بیمارستان بستری شد
- او من را تهدید و مجبور به اعمال جنسی تحقیر آمیز کرد؛ اعترافات تکان دهنده نامزد ستاره سابق وستهام
- پس از شکستن رکورد: رئیس اف بی آی با اوچکین دیدار میکند
- استندآپ کمدین معروف به دلیل بستنی تمام شب را در بیمارستان گذراند
- شکیرا فاش میکند که چگونه بر خیانت پیکه غلبه کرده است
- سه روز پس از تبرئه آلوز| همسرش او را با خبر خوشحال کننده شگفت زده میکند
- جوانترین قهرمان جهان در مورد فواید شطرنج برای کودکان صحبت میکند
- حبیب نورمحمدوف خود را به یک "ماشین" تشبیه میکند و مبارزان تیمش را با برندهای معروف خودرو مقایسه میکند
- آنها میخواهند مرا در چک بکشند| مربی سابق زنیت عدم امکان حضور در صدمین سالگرد باشگاه روسی را توضیح میدهد
- از ستاره سابق لیورپول تا کار به عنوان یک تمیز کننده فاضلاب
- ستاره الاتحاد عربستان با تعجب گفت: قبل از تبدیل شدن به یک بازیکن مشهور زباله جمع آوری میکردم
- کتاب: کیت میدلتون با شاهزاده ویلیام "به عنوان چهارمین فرزندش" رفتار میکند
- فرح الفاسی، خواننده مشهور مراکشی، اسرار طلاق و تفکر خودکشی قبلی خود را فاش میکند
- افشاگری پزشکی هیجان انگیز، رمز و راز مرگ بتسی آراکاوا، همسر بازیگر آمریکایی جین هکمن را افزایش میدهد
- هبه ابوک به اظهارات همسر سابقش اشرف حکیمی پاسخ میدهد
- "از ترس خیانت دوستش"پ انزو فرناندز به دنبال بازگرداندن نامزد سابقش است
- عکس| ایمان خلیف یک هدیه "فوق العاده" از یک بازیکن رئال مادرید دریافت میکند
- واکنش بنزما به اظهارات رونالدو که خود را "بزرگترین تاریخ " مینامد!
- "حمایت خانواده"| مادربزرگ یامینه یامال در جایگاههای بارسلونا کانون توجه را به خود جلب میکند + تصاویر
- وضعیت شرم آور برای بازیکن آرسنال به دلیل ستاره یک برنامه دوستیابی محبوب
- عکس| رونالدو با یک نظر خوب با سی و نهمین سال خود خداحافظی کرد
- در یک موقعیت خنده دار و شرم آور| یک هوادار بادیگارد مسی را به زمین میزند! + ویدئو
- بدر هاری قهرمان مراکشی در آمستردام دستگیر شد
- ویدئو| نیمار دلایل جدایی خود از الهلال را فاش کرد
- عکس| اشتباه املایی هالند درباره اسم خرید جدید سیتیزنها مورد تمسخر قرار گرفت!
- داستان عمر مرموش و تیم ملی کانادا چیست؟
- متهم اصلی حمله چاقو به سیف علی خان ستاره بالیوود دستگیر شد
- علیرغم دخالت او در یک "رسوایی جنسی"| بازیکنی پس از اینکه واندا نارا با شوهرش به او خیانت کرد، به دنبال غرامت است
- حمایت بانکها از بازار سرمایه از فردا اجرا میشود
- بورس سقوط کرده در دولت روحانی چگونه در دولت شهید رئیسی احیا شد؟
- درمان بورسی پزشکیان از زبان عبده
- جذب سرمایه ۷ همتی از بازار بورس دانشبنیانها
- وعده عناب بورسی واقعیتر شد
- چهارمین روز نزولی بازار در غیاب نیروهای صعودی
- انتخابات و دامنه نوسان مهمترین دلیل رکود فعلی بورس
- بورس با ۴ مصوبه دولت برای حمایت از بازار سهام سبزپوش میشود؟
- ۳ دلیل پایین بودن ارزش معاملات خرد در بورس
- معافیتهای مالیاتی بازار سرمایه باید استمرار پیدا کند
- بورس این روزها تحت تأثیر تداوم نرخ اخزای بالای ۳۵ درصد
- رشد شاخصهای بورس با کف سازی تکنیکال
- کاهش دامنه نوسان هم علاج بورس نزولی نبود
- سایه تامین مالی دولت بر سر بورس سنگینی میکند
- کاهش بی سابقه حجم معاملات سهام در بورسهای جهانی
- رشد شاخصهای بورس با کمک بانکیها و اعلام نرخ تسعیر ارز
- حمله به سفیر روسیه در لهستان
- معرفی سری گوشیهای Redmi K ۵۰ قبل از رونمایی رسمی
- غفوری: فکر کردن به قهرمانی از الان، سادهلوحانه است
- کاهش ۱۰ درصدی تولید هوندا در دو کارخانه
- سومین نشست دستمزد، باز هم بدون نتیجه
- لغو بلیت فروشی عمومی المپیک زمستانی چین
- گرامیداشت قربانیان هواپیمای اوکراینی در دانشگاه تورنتو
- ادامه چانهزنی چهارگانه در وین
- صرفهجویی ۱.۶ میلیارد دلاری کمیته برگزاری المپیک و پارالمپیک توکیو
- محبوبترین رشته المپیک توکیو مشخص شد
- اعلام هزینه میزبانی توکیو از المپیک و پارالمپیک ۲۰۲۰،
- آذرتاج: هیات اقتصادی جمهوری آذربایجان به ایران میرود
- بررسی عملکرد ایران در المپیک؛ جایگاه چهارمی در آسیا
- پایان وضعیت اضطراری در کشور میزبان المپیک ۲۰۲۰
- آرایشی که مرز سلامتی را رد کرد! چرا ما هاب زیبایی نشویم؟
- چرا «تاسیان» با هیاهو هم به گرد «خاتون» نرسید؟
- چرا فرانچسکو خطرناکتر از قبل است؟!
- «مرجان» و یک راز مگوی؟ زنانهگویی ازدواج اجباری
- گرافیکی جاودانه از تجریش
- «سووشون» لرزان لرزان آمد
- روایت آرتیستهای جا مانده از قافله
- غزه دلخراش: کودکانی که از گرسنگی شدید قادر به گریه کردن نیستند، در آغوش والدین خود جان میدهند، در حالی که جهان با وحشت و ترس نظارهگر این صحنه است
- آب با لیمو صبح ناشتا: همه به آن نیاز ندارند
- علت جدید سرطان تهاجمی در زنان جوان کشف شد
- EADV: داروهای کاهش وزن در مبارزه با هیدرآدنیت چرکی کمک میکنند
- به افراد مبتلا به آلرژی هشدار داده شد که روی چمن دراز نکشند
- چین داروهای جدید ضد چاقی با فواید متعدد برای قلب و کبد تولید میکند
- نوشیدنی ضد چروک: مطالعه نشان میدهد که وضعیت پوست بهبود مییابد
- ۹۶ درصد اقیانوسها در حال «جوشیدن» هستند| یک مطالعه جدید از یک فاجعه اقلیمی خبر میدهد
- Health: وضعیت خوابیدن میتواند تأثیر قابل توجهی بر سلامت مغز داشته باشد
- دانشمندان دریافتهاند چه چیزی به حفظ رگهای خونی در طول سبک زندگی بیتحرک کمک نمیکند
- اسید جدید در باران ظاهر میشود| چقدر خطرناک است؟
- کمبود ویتامین B۶ خطر ابتلا به دیابت نوع ۲ را افزایش میدهد
- چین کریستال غولپیکر BGSe را توسعه میدهد که در تولید سلاحهای لیزری فوق قدرتمند مورد استفاده قرار میگیرد
- افراد سیگاری و ویپر تغییرات DNA مشابهی دارند که با سرطان مرتبط است
- خواص گرافیت مورد استفاده در فضاپیما
- یک کشف مهم، افقهای جدیدی را در مبارزه با سرطان پروستات تهاجمی میگشاید
- متخصص، بازیهای صوتی را برای کاهش خطر زوال عقل توصیه میکند
- شایعترین غذاهای حساسیتزا و علل واکنش به آنها
- Brain: اثرات TBI میتواند برای دههها ادامه داشته باشد
- سر و صدای هواپیما در شب با اختلال خواب مرتبط است
- وجود برخی تومورها| علل سوزش دست
- اندازهگیری شکل بدن به پیشبینی خطر بیماری قلبی کمک میکند
- بهترین و بدترین میوهها از نظر ارزش غذایی
- تودههای زیر پوست میتوانند اولین نشانه سرطان باشند
- مطالعه: استفاده بیش از حد از ردیابهای تناسب اندام ممکن است سلامت را بدتر کند
- ۵ نشانه که بدن شما در حال مبارزه با یک بیماری نامرئی است
- کولگاوچوک: افزایش موارد اسکیزوفرنی با «فشار اطلاعاتی قوی» مرتبط است
- یک برنامه ورزشی جدید، درد آرتروز را در عرض دو ماه تسکین میدهد
- حفظ تعادل روانی-عاطفی| روانشناس آندریوا توصیههایی در مورد چگونگی مقابله با افسردگی و اضطراب ارائه داد
- برای حفظ بهداشت، ملحفهها را هر چند وقت یکبار باید شست؟
- خوردن صبحانه زودهنگام و ناشتا بودن در طول شب میتواند از افزایش وزن جلوگیری کند
- کارشناسان فاش کردند که کدام شیر فایدهای ندارد
- اخبار داغ
- ورزشی
- پربیننده
- پربحث
- والوکوردین و کوروالول میتوانند باعث حمله قلبی و اعتیاد شوند
- وزیر امور خارجه مجارستان درخواست بوداپست در مورد درگیری اوکراین را یادآوری کرد
- هریس «قانون را زیر پا گذاشت» | ترامپ تهدید میکند: جهنم به پا خواهد شد، زیرا دموکراتها مبالغ هنگفتی برای حمایت میپردازند
- واشنگتن پست: کشورهای اروپایی سازوکار جدیدی برای ارسال سلاح به اوکراین ایجاد کردهاند
- رئیس پنتاگون از استفاده از دروغ سنج برای یافتن افشاگران رسانهای منع شد
- پزشک بیماری جدیدی را که ناشی از سیگار الکترونیکی است، شناسایی کرد
- یک فاجعه انسانی: پزشکان غزه از گرسنگی در اتاقهای عمل از حال میروند
- نیروگاه زاپوروژیه: حملات اوکراین تهدیدی «بسیار بالا» برای ایمنی هستهای است
- وزیر امور خارجه آمریکا فاش کرد که واشنگتن چه نوع رابطهای را با پکن آرزو دارد
- تراژدی هوایی به معما تبدیل شد: جسد مسافر هندی پس از فرود هواپیما ناپدید شد!
- اکسیوس: دموکراتهای کنگره به دنبال دسترسی به کتاب تولد ۵۰ سالگی جفری اپستین هستند
- سونی قصد دارد بازیهای خود را برای سایر کنسولها و گوشیهای هوشمند منتشر کند
- دارویی ساخته شده است که سلولهای سرطانی را به روشی خاص از بین میبرد
- باران شدید تایلند و کامبوج را مجبور به آتشبس موقت کرد
- اطلاعات شخصی کاربران اپلیکیشن نقد و بررسی مردان به صورت آنلاین فاش شد
- یک "محافظ" برای لوزالمعده در بدن انسان یافت شد
- اسلاتسکی: ائتلاف موسوم به ائتلاف مشتاقان، دیوانهوار به دنبال تشدید روابط بین روسیه و ناتو است و بر طبل جنگ میکوبد
- ارتش اسرائیل روز جمعه مرتکب قتل عام کسانی شد که در خان یونس در انتظار روزی بودند
- مایعات موجود در چمدانهای دستی در اروپا تعویض میشوند
- دانشمندی فاش میکند که واقعاً چند وقت یکبار باید حولهها را بشویید
- تلاشهای مصر و قطر برای افزایش کمک به غزه و بازگشایی گذرگاههای بیشتر
- سودان از سازمان ملل متحد میخواهد که برای جلوگیری از جنایات نیروهای پشتیبانی سریع، اقدامات قاطعی انجام دهد
- رئیس جمهور صربستان از قول شی جین پینگ به خود پرده برداشت
- ترامپ از دست دادن ۱۰۰ میلیون دلار جمعآوریشده برای قربانیان آتشسوزی کالیفرنیا را اعلام کرد
- اوربان فاش کرد که اگر جای فون در لاین بود چه میکرد
- روش جدیدی برای درمان هدفمند سرطان ابداع شد
- پاتروشف: ملوانان ما قبلاً ناوگان نازی را شکست دادهاند
- کاخ سفید: ترامپ همچنان برای گفتوگو با رهبر کره شمالی آماده است
- به WP گفته شد که چگونه اروپا از آمریکا برای اوکراین سلاح خریداری خواهد کرد
- دانشمندان متوجه تغییر در محور چرخش پوسته زمین شدهاند
- پاتروشف: مرتس نظامیگری آلمان را با بهترین سنتهای رایش سوم توجیه میکند
- کارشناس، قصد کییف برای افتتاح سفارتخانه در آمریکای لاتین را ارزیابی میکند
- متخصص مغز و اعصاب راههایی برای کاهش سرعت پیشرفت زوال عقل ارائه میدهد
- نظرسنجی: دموکراتها در پایینترین سطح حمایت عمومی در ۳۵ سال گذشته قرار دارند
- ایالات متحده خدمت سربازی را از وضعیت ۱۰ به وضعیت ۳۲ تغییر میدهد
- روسها لابوبو را به آیفون ترجیح میدهند
- یک پزشک از خطر مسمومیت با هود آشپزخانه گفتند
- سودان: فاجعه انسانی در الفاشر و کمبود تقریباً کامل مواد غذایی
- عضلات مصنوعی برای پیوند در روسیه ساخته شدند
- یک آژانس فاش کرد که به دلیل قطع سرویس استارلینک چه اتفاقی برای نیروهای اوکراینی افتاده است
- برای جلوگیری از منچستر سیتی، بارسلونا بازیکن خود را با قراردادی بلندمدت به خدمت گرفت
- رسانهها پیش از دیدار فون در لاین و ترامپ از تردیدها و بیاعتمادی در اتحادیه اروپا مطلع شدند
- داروهای محبوب کاهش وزن یک نقص جدید دارند
- جنبش نافرمانی فرانسه: به رسمیت شناختن فلسطین توسط مکرون کافی نیست و ما خواستار مداخله نظامی فرانسه هستیم
- اوربان اتحادیه اروپا را به حمایت از درگیری در اوکراین متهم کرد
- ترکیب صبحانه ایدهآل مشخص شد
- رئیس سابق اداره مبارزه با فساد اوکراین درباره محدود کردن فعالیتهای این نهاد اظهار نظر کرد
- نوجوانان آمریکایی شروع به جایگزینی دوستان خود با شبکههای عصبی کردهاند
- دانشمندان کشف کردهاند که چرا افراد مسن در «خواندن» احساسات بهتر عمل میکنند
- فیدان: توافق اولیه برای برگزاری اجلاسی در ترکیه با حضور پوتین، زلنسکی، اردوغان و ترامپ حاصل شده است
- زاخارووا: نهادهای مبارزه با فساد اوکراین هیچ ارتباطی با مبارزه با فساد ندارند!
- اوربان: عضویت اوکراین در اتحادیه اروپا منجر به جنگ با روسیه خواهد شد
- دانشمندان کشف کردهاند که کدام ایمپلنتها میتوانند روند بهبود استخوان را تسریع کنند
- والدین از خطرات اردکهای پلاستیکی برای حمام کردن مطلع شدند
- مشخص شده است که چه زمانی رگهای مغزی به "متحدان" زوال عقل تبدیل میشوند
- دانشمندان پرم یک عامل خطر ناشناخته برای سکته مغزی را شناسایی کردند
- دانشمندان دریافتند که کافئین ممکن است با آنتیبیوتیکها تداخل داشته باشد
- خطر پنهان کمبود ویتامین D کشف شد
- ترامپ: اوباما در مدیریت اطلاعات مربوط به روسیه مرتکب جرم شده است
- ترامپ از حق عفو همدست اپستین میگوید
- ترامپ به مقامات اروپایی در مورد اتفاقی وحشتناک هشدار داد: خودتان را جمع و جور کنید وگرنه دیگر اروپایی نخواهید داشت
- نخست وزیر بریتانیا نسبت به خطرات سفر ترامپ هشدار داد
- معاون رئیس شورای فدراسیون روسیه: حل و فصل مسالمتآمیز بحران اوکراین، مرگ سیاسی زلنسکی و اطرافیانش خواهد بود
- بلومبرگ جزئیات غیرمنتظرهای از مکالمه ترامپ و استارمر را فاش کرد
- دانشمندان کشف کردهاند که چه زمانی آلرژی میتواند از سرطان ریه جلوگیری کند
- سیاستمدار اوکراینی: تنها گزینه برای آینده مردم اوکراین، پیوستن به روسیه خواهد بود
- مشخص شد چه کسی ترامپ را متقاعد کرد تا ارسال سامانه دفاع هوایی به اوکراین را از سر بگیرد
- شیر بز برای سالمندان مفید است
- یک پزشک روش صحیح مصرف چندین دارو در روز را توضیح میدهد
- رئیس کمیسیون اروپا پیش از اعمال تعرفهها، در اسکاتلند با ترامپ درباره روابط تجاری گفتوگو خواهد کرد
- رئیس جمهور آمریکا درباره توافق تجاری اتحادیه اروپا و آمریکا اظهار نظر کرد
- دانشمندان دلیل «گرسنگی ابدی» پس از رژیمهای غذایی سخت را کشف کردند
- رسانههای آمریکایی گزارش میدهند که چه چیزی واشنگتن را وادار خواهد کرد تا کیف را مجبور به دادن امتیاز به مسکو کند
- ترامپ در حال بررسی صدور چکهای بازپرداخت نقدی برای آمریکاییها از محل عوارض گمرکی است
- نخست وزیر لهستان به داشتن رابطه نامشروع با وزیر آموزش و پرورش نوواکا مظنون است
- سازمان ملل: بیش از ۱۳۱ هزار نفر در تایلند و بیش از ۴۰۰۰ نفر در کامبوج از خانههای خود آواره شدهاند
- شرکت دفاعی آلمانی دل از قانون تسریع تسلیحات استقبال میکند
- دو داروی سرطان، پیشرفت بیماری آلزایمر را کند میکنند
- نماینده مجلس اوکراین: کیف بودجه لازم برای تشویق بازگشت پناهندگان به کشور را ندارد
- صربستان موافقت خود با تحریمهای روسیه را در ازای تضمین عضویت در اتحادیه اروپا معامله میکند
- Takvim: زنیت برای رنان ۱۵ میلیون یورو ارزش قائل است، بشیکتاش میخواهد این مدافع را بخرد
- نقطه عطف سوپرلیگ: «اصل توافق با یوفا»
- بوکما-اندویه، خط مستقیم و جذابیتهای بازار نقل و انتقالات: "من هر روز با او تماس میگیرم. "
- سود سرمایه هنوز تمام نشده است: طوفان جدیدی بین ناپولی و یوونتوس از راه میرسد
- رومانو: فنرباغچه پیشنهاد انتقال اشکرینیار را بهبود میبخشد
- یوونتوس آماده معاوضه خط میانی با رم است
- اسلات، سرمربی لیورپول، معتقد است که تیمش نیازی به خرید مدافع میانی ندارد
- طارمی-اینتر، رابطهای که هرگز شکوفا نشد| طارمی، اینتر چراغ سبز نشان داده است: این اتفاقی است که دارد میافتد
- ماریانوچی از ناپولی شگفتزده شد: «میخواستم با بهترین تیمهای ایتالیا بازی کنم.»
- دوناروما در سری آ: همه چیز تغییر میکند، پاری سن ژرمن یک جایگزین دارد
- لواندوفسکی پاسخ داد که بارسلونا برای قهرمانی در لیگ قهرمانان اروپا به چه چیزهایی نیاز دارد
- GMS: منچستریونایتد برای فروش گارناچو که مورد توجه چلسی و ناپولی است، ضربالاجل تعیین کرد
- فوتمرکاتو: گالاتاسرای به دوناروما پیشنهاد داد
- غافلگیری چالهان اوغلو: احتمال انتقال از بین نرفته است
- تصمیم قاطع رئال مادرید در مورد رینیر
- امضای قراردادی که ویارئال در حال نهایی کردن آن است
- رومانو: خیرونا با انتقال قرضی لمار از اتلتیکو موافقت کرد
- آرن اسلات در مورد لزوم خرید تعداد زیادی بازیکن در این فصل توضیح داد
- آنتالیا اسپور ترکیه از انتقال جورجی ژیکیا خبر داد
- مشکل جدیدی برای رودریگو ایجاد میشود
- پیشنهاد جدید ۱۴ میلیون یورویی برای آندری رتیو
- ویکتور گیوکرس با بیش از ۷۰ میلیون قرارداد امضا کرد
- بازیکن بسکتبال آمریکایی یکی از باشگاههای NBA را با رئال مادرید مقایسه میکند
- این مدافع که در زمستان به منچسترسیتی پیوست، ممکن است به خیرونا برود
- میکل آرتتا در مورد انتقال گیوکرس به آرسنال صحبت میکند
- دو خریدی که سویا در حال مذاکره با آنهاست
- پی اس جی قرارداد جذب دروازه بان را امضا کرد!
- سرمربی لیورپول دلیل کنار گذاشتن دیاز از بازی مقابل میلان را فاش کرد
- ناپولی دروازهبان جدیدی به خدمت گرفت
- فن دایک، مدافع لیورپول: باید به تدریج به فرم ایده آل برسیم
- گیوکرس: مشتاقم عضوی از آرسنال باشم و با این لباس گلزنی کنم
- باشگاه لیدز یونایتد اعلام کرد لوکاس پری، دروازهبان لیون را به خدمت گرفته است
- تعهد کامل به جولیان آلوارز
- رئال بتیس میخواهد قراردادش را ارزانتر کند
- آنها از یک تغییر اساسی با رائول آسنسیو خبر میدهند
- فن دایک، مدافع لیورپول: همه خریدهای جدید ارزش خود را نشان دادهاند، اوضاع حتی بهتر هم خواهد شد
- پاری سن ژرمن جانشین دوناروما را انتخاب کرد
- گیوکرس توضیح میدهد که چرا تصمیم گرفت به آرسنال بپیوندد
- پارما میخواهد در دورتموند ماهیگیری کند
- منچسترسیتی پیشنهاد ۶۰ میلیون یورویی خود را از سر گرفت
- مهمان جدیدی برای جیو سیمئونه
- مدافع لیورپول، فن دایک: من قبلاً هرگز به هنگ کنگ نرفتهام، عالی است
- میلینکوویچ ساویچ، دروازهبان تورینو، به صورت قرضی به ناپولی پیوست
- آ بولا: اسپورتینگ به دنبال جذب مدافع اسپارتاک است
- پیشنهاد غیرمنتظره برای جانلوئیجی دوناروما
- چرخش رادیکال با ماریو هرموسو
- نوسازی که باشگاه بارسلونا فوراً به آن نیاز دارد
- دفنسا سنترال: رئال مادرید به فروش وینیسیوس فکر میکند
- MSN: آندری لونین میتواند به منچستریونایتد برود
- گرمیو برای تقویت تیم، بین وندل و ملو، بازیکن یوونتوس، یکی را انتخاب میکند