- ارتباط با ما
- |
- درباره ما
- |
- نظرسنجی
- |
- اشتراک خبری
- |
- نگارنامه
دانشمندان روش جدیدی برای چاپ سهبعدی رگهای خونی ابداع کردند
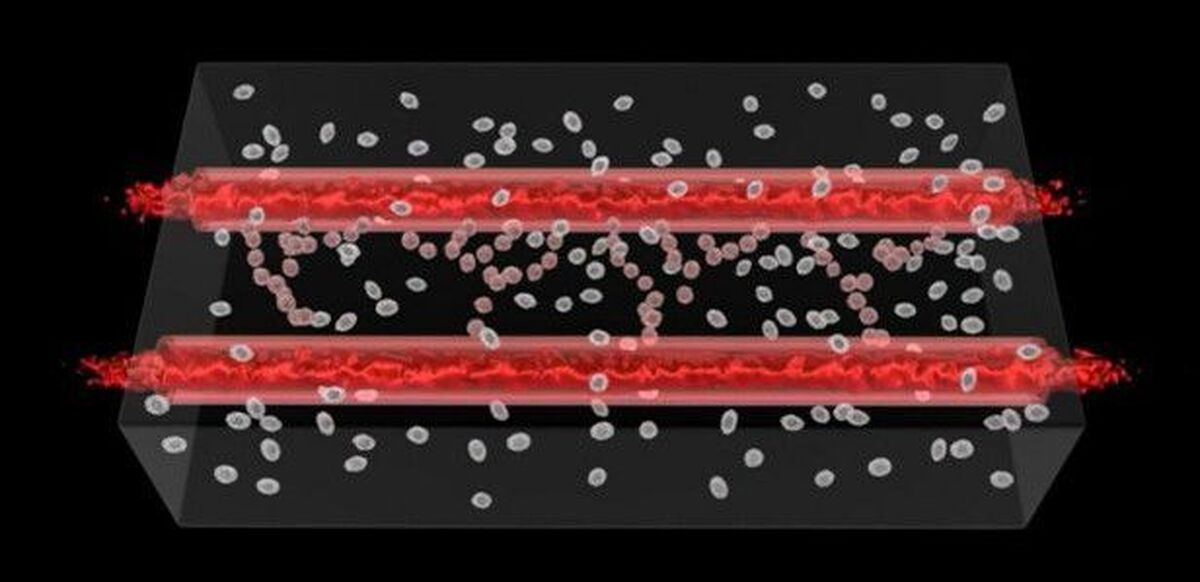
به گزارش مجله خبری نگار، پرورش اندامهای کارآمد انسان در خارج از بدن، «جام مقدس» دیرینه پزشکی پیوند عضو است که همچنان دستنیافتنی باقی مانده است. تحقیقات جدید موسسه مهندسی زیستی ویس هاروارد و دانشکده مهندسی و علوم کاربردی جانای. پالسون (SEAS) این تلاش را یک گام بزرگ به تکمیل نزدیکتر میکند.
تیمی از دانشمندان روش جدیدی برای چاپ سهبعدی شبکههای عروقی ایجاد کردهاند که از رگهای خونی به هم پیوسته با یک "پوسته" ویژه از سلولهای ماهیچه صاف و سلولهای اندوتلیال احاطهکننده یک "هسته" توخالی که از طریق آن سیال میتواند جریان یابد، تشکیل شده و در بافت قلب انسان جاسازی شده است. این معماری عروقی به دقت از رگهای خونی طبیعی تقلید میکند و پیشرفت قابل توجهی را در جهت امکان تولید اندامهای انسانی قابل کاشت نشان میدهد. این دستاورد در مجله Advanced Materials منتشر شده است.
پاول استنکی، نویسنده اول مقاله، گفت: «در کار قبلی، ما یک روش جدید چاپ زیستی سهبعدی به نام نوشتن قربانی در بافت عملکردی (SWIFT) را برای ایجاد کانالهای توخالی در یک ماتریکس سلولی زنده توسعه دادیم. در اینجا، با تکیه بر این روش، SWIFT هممحور (co-SWIFT) را ارائه میدهیم که معماری چندلایه موجود در رگهای خونی طبیعی را تکرار میکند و تشکیل اندوتلیوم به هم پیوسته را تسهیل کرده و مقاومت آن را در برابر فشارهای جریان خون داخلی افزایش میدهد.»
نوآوری کلیدی توسعهیافته توسط این تیم، یک نازل منحصربهفرد هسته-پوسته با دو کانال سیال قابل کنترل مستقل برای «جوهر» تشکیلدهنده رگهای چاپشده بود: یک جوهر پوسته کلاژنی و یک جوهر هسته ژلاتینی. محفظه داخلی نازل هسته کمی فراتر از محفظه پوسته بیرون زده است، به طوری که نازل میتواند رگ چاپشده قبلی را به طور کامل سوراخ کند تا شبکههای به هم پیوسته و شاخهدار برای اکسیژنرسانی کافی به بافتها و اندامهای انسانی از طریق پرفیوژن ایجاد کند. اندازه رگها را میتوان در حین چاپ با تغییر سرعت چاپ یا سرعت جریان جوهر تغییر داد.
برای اعتبارسنجی روش جدید co-SWIFT، این تیم ابتدا رگهای چندلایه خود را در یک ماتریس هیدروژل شفاف و دانهای چاپ کردند. سپس رگها را در یک ماتریس تازه ایجاد شده به نام uPOROS چاپ کردند که از یک ماده متخلخل مبتنی بر کلاژن ساخته شده است که ساختار فیبری متراکم بافت ماهیچه زنده را تکرار میکند. آنها توانستند با موفقیت شبکههای عروقی گستردهای را در هر دوی این ماتریسهای بدون سلول چاپ کنند. پس از چاپ این رگهای بیومیمتیک، ماتریس گرم شد که باعث شد کلاژن موجود در ماتریس و جوهر پوسته به هم متصل شوند و جوهر هسته ژلاتینی قربانی ذوب شود و به راحتی قابل جدا شدن باشد و یک شبکه عروقی باز و نفوذپذیر ایجاد شود.
این تیم با حرکت به سمت مواد بیولوژیکی مرتبطتر، فرآیند چاپ را با استفاده از جوهر پوستهای که با سلولهای ماهیچه صاف (SMC) پر شده بود، تکرار کردند. این سلولها لایه بیرونی رگهای خونی انسان را تشکیل میدهند. پس از ذوب جوهر هسته ژلاتینی، آنها سپس سلولهای اندوتلیال (EC) را که لایه داخلی رگهای خونی انسان را تشکیل میدهند، به داخل عروق آنها تزریق کردند. پس از هفت روز تزریق، هم SMCها و هم ECها زنده بودند و به عنوان دیواره رگ عمل میکردند - آنها شاهد کاهش سه برابری نفوذپذیری عروق در مقایسه با نمونههای بدون SMC بودند.
در نهایت، آنها آماده بودند تا روش خود را درون بافت زنده انسان آزمایش کنند. آنها صدها هزار بلوک سازنده اندام (OBB) - کرههای کوچکی از سلولهای ضرباندار قلب انسان که در یک ماتریکس سلولی متراکم فشرده شدهاند - را مهندسی کردند. سپس، با استفاده از co-SWIFT، یک شبکه بیومیمتیک از رگها را روی بافت قلب چاپ کردند. در نهایت، آنها جوهر هسته قربانی را حذف کردند و داخل رگهای مملو از SMC خود را از طریق پرفیوژن با EC کشت دادند و عملکرد آنها را ارزیابی کردند.
این رگهای زیستتقلیدی چاپشده نهتنها ساختار دولایه مشخصه رگهای خونی انسان را نشان دادند، بلکه پس از پنج روز تزریق با مایعی که خون را تقلید میکرد، OBBهای قلبی شروع به ضربان هماهنگ کردند که نشاندهنده بافت قلبی سالم و عملکردی بود. این بافتها همچنین به داروهای قلبی رایج پاسخ دادند - ایزوپروترنول باعث شد آنها سریعتر ضربان بزنند، در حالی که بلبیستاتین آنها را متوقف کرد. این تیم حتی مدلی از عروق گسترده شریان کرونری چپ یک بیمار واقعی در OBB را بهصورت سهبعدی چاپ کرد و پتانسیل آن را برای پزشکی شخصیسازیشده نشان داد.
لوئیس، که همچنین استاد مهندسی زیستی هانسیورگ ویس در SEAS است، گفت: «ما توانستیم با موفقیت مدلی از عروق شریان کرونر چپ را بر اساس دادههای واقعی بیمار، به صورت سهبعدی چاپ کنیم که نشاندهندهی کاربرد بالقوهی co-SWIFT برای ایجاد اندامهای انسانی عروقی مختص بیمار است.»
تیم لوئیس قصد دارد در کارهای آینده، شبکههای مویرگی خودسازمانده ایجاد کند و آنها را با شبکههای رگهای خونی چاپ سهبعدی ادغام کند تا ساختار رگهای خونی انسان را در مقیاس میکروسکوپی دقیقتر شبیهسازی کند و عملکرد بافتهای رشد یافته در آزمایشگاه را بهبود بخشد.
«دونالد اینگبر»، یکی از نویسندگان این مطالعه، گفت: «گفتن اینکه ایجاد بافت زنده و کاربردی انسان در آزمایشگاه چالشبرانگیز است، کم لطفی است. من به عزم و خلاقیتی که این تیم در اثبات توانایی خود در ایجاد رگهای خونی بهتر در بافت قلب زنده و تپنده انسان نشان داده است، افتخار میکنم. مشتاقانه منتظر موفقیتهای مستمر آنها هستم، زیرا آنها به دنبال روزی هستند که بافت رشد یافته در آزمایشگاه را به بیماران پیوند بزنند.»
- لطفا از نوشتن با حروف لاتین (فینگلیش) خودداری نمایید.
- از ارسال دیدگاه های نا مرتبط با متن خبر، تکرار نظر دیگران، توهین به سایر کاربران و ارسال متن های طولانی خودداری نمایید.
- لطفا نظرات بدون بی احترامی، افترا و توهین به مسئولان، اقلیت ها، قومیت ها و ... باشد و به طور کلی مغایرتی با اصول اخلاقی و قوانین کشور نداشته باشد.
- در غیر این صورت، «نگارمگ » مطلب مورد نظر را رد یا بنا به تشخیص خود با ممیزی منتشر خواهد کرد.




- آخرین اخبار
- محبوب
- برچسب های داغ
- دانشمندان کشف کردهاند که برای محافظت از خود در برابر افسردگی، چند وقت یکبار باید رابطه جنسی داشته باشید
- «روزه ساختگی» ... روشی عملی برای جوانسازی سلولها بدون رژیم غذایی سخت!
- بنزما در مورد رونالدو: ما به یکدیگر احترام میگذاریم، نیازی نیست برای دوربین بازی کنیم
- بازیکن فنرباغچه به دلیل استفاده از تصاویر هری پاتر تحت پیگرد قانونی قرار گرفت
- بهترین زمان برای خوردن شام در زمستان
- او چقدر درآمد خواهد داشت؟ … مصاحبه با ترامپ ثروت کریستیانو رونالدو را افزایش میدهد
- یک متخصص تغذیه فاش کرد که کدام قارچها انرژی جنسی را تقویت میکنند
- باشگاه فوتبال بیرمنگام سیتی قصد دارد یک ورزشگاه ۶۲۰۰۰ نفری با ۱۲ دودکش بسازد
- سطح خواندن و ریاضی دانشآموزان آمریکایی پس از همهگیری کووید-۱۹ همچنان رو به کاهش است
- با وجود بوی تندش! دهانشویه حاوی سیر ممکن است از ضدعفونیکنندههای رایج بهتر عمل کند
- ماسک درباره آینده گردش پول با توسعه هوش مصنوعی صحبت کرد
- عادت بدی که باعث ریزش مو و سفیدی زودرس مو میشود
- لیونل مسی در طول تور هند خود برای هر بازی تا سقف ۱۰۷۰۰۰ دلار دریافت خواهد کرد
- خطرات استفاده روزانه از سشوار
- تعداد بیسابقهای از زنان| از هر پنج آمریکایی، یک نفر میخواهد ایالات متحده را ترک کند
- وقتی اسپانیول سعی کرد لئو مسی را جذب کند...
- فیلم| وزیر معادن کنگو از سقوط هواپیما جان سالم به در برد
- شبکه تلویزیونی ترکیه: علت مرگ گردشگران آلمانی در استانبول، سمی بود که پادزهری نداشت
- مطالعهای ارتباط بین درآمد و زوال عقل را کشف کرد
- ماروتا: برای عاشقان قدیمی، فکر تخریب سن سیرو تلخی و نوستالژی را تداعی میکند
- مزایا و معایب خوردن کافئین در بارداری!
- باتریهای جدید با ویژگیهای بهتر و کارآمدتر!
- معضل مصرف بیرویه آنتیبیوتیک در ایران به مرز هشدار رسید!
- سالمندان در خصوص تغذیه و فعالیت بدنی این موارد را باید رعایت کنند!
- چربی احشایی چه زمانی برای سلامتی مضر است؟
- وجود حس هفتم در حال تایید است!
- گوشت دایناسورها قبلا قابل خوردن بوده است؟
- چشم سوم چیست؟ چه کاربردی دارد؟
- کشف سنگی عجیب و نادر در مریخ توسط مریخنورد «استقامت»!
- آشنایی با چالشهای زنان در دوران یائسگی!
- هورمون استرس در مادر منجر به رویش سریع دندانهای نوزاد میشود!
- هنگام سرگیجه از مصرف این ۴ گروه غذایی دوری کنید!
- بینی بر رفتار ما تاثیر دارد!
- فعالیت کوتاه چند دقیقهای استرس را کم میکند!
- پنومونی همچنان تهدید جدی برای کودکان و سالمندان!
- رشد مجدد مو به کمک روغن رزماری!
- غلبه بر غم و افسردگی با سادهترین راهکارها!
- سه تغییر کلیدی برای کاهش ابتلا به دیابت نوع ۲!
- کافئین عوارض جانبی دارد؟
- سلولهای بنیادی به کمک ترمیم شکستگیهای ناشی از پوکی استخوان میآیند!
- واکر مخصوص کودکان فلج مغزی ساخته شد!
- درمان دیابت نوع یک ممکن میشود!
- همهگیری بیماریهای مزمن زیر سر غذاهای فوق فرآوریشده است!
- نقش ژنهای مؤثر در ابتلا به سرطان سینه!
- واکسیناسیون آنفلوآنزا برای چه کسانی ضروری است؟
- پیرگوشی در دوران میانسالی چه تاثیری بر زندگی دارد؟
- تب برفکی دامها میتواند وارد چرخه غذایی مردم شود؟
- شایعترین عامل عفونتهای حاد تنفسی چه هستند؟
- وعدههای غذایی دیرهنگام چه تاثیری بر سلامتی دارند؟
- پنج آزمایش واجب برای مردان و زنان پس از چهل سالگی!
- غذاهای فوق فرآوریشده میتوانند باعث دیابت شوند!
- بیماران مبتلا به زخم معده تا چه زمانی نیاز به دارو دارند؟
- بررسی پراکندگی جغرافیایی مصرف آنتیبیوتیکها در کشور!
- نسبت به محصولات تبلیغ شده به عنوان محرک بانوان هوشیار باشید!
- قیمت مکملها و شیرخشک سازمان غذا و دارو چقدر است؟
- مقاومت میکروبی چالش جدید سازمان جهانی بهداشت!
- پوست شما از دیابت خبر میدهد!
- درمان شخصیسازیشده مرگ بخاطر سرطان ریه را از بین میبرد!
- برای کاهش یا رفع ریزش مو چه میتوان کرد؟
- برای حفظ فشار خون سالم چی بخوریم؟
- یک سیستم پلیمری ابر مولکولی که با شدت نور ساختارش تغییر میکند!
- چطور برخی از افراد در به خاطر سپردن چهرهها استاد هستند؟
- یک سیستم هشدار عمومی برای ارسال پیامهای اضطراری!
- شتابدهندهای میکروسکوپی تولید پرتوهای ایکس را ممکن کرد!
- ۳ ماهواره سنجشی ایرانی در دی ماه به فضا میروند!
- زنان باردار واکسیناسیون آنفلوآنزا را جدی بگیرند!
- تولید هیدروژن سبز ممکن شد!
- این ۶ شش نشانه خبر از مشکلات جدی حافظه میدهند!
- توسعه نسل تازهای از موشکهای ضدکشتی با کمک هوش مصنوعی!
- بهترین انتخاب برای رفع یبوست مزمن چیست؟
- رفتوآمد زنبورها چگونه انجام میشود؟
- نایابترین گروه خونی را بشناسید!
- ریتم شبانهروزی بدن چگونه کار میکند؟
- نوشیدن الکل از جمله دلایل ابتلا به سکته!
- ارتباط بین میزان آلودگی ناشی از سوسکها و افزایش سطح آلرژنها!
- کاهش تدریجی حافظه کوتاهمدت با این علائم همراه است!
- چه کنیم تا از سکته در امان بمانیم؟
- راهی تازه برای مقابله با انگلها به کمک میکروبهای تکسلولی!
- کشف نانوکریستالهای مونازیت در گیاه سرخس!
- بازیافت ایمن باتریهای لیتیوم-یون به کمک علم رباتیک!
- رسوایی تکاندهنده درباره یک میلیاردر جهانی: او عاشق جفری اپستین، مجرم جنسی، بود، اما!
- جنیفر لارنس توضیح داد که چرا دیگر از ترامپ انتقاد نمیکند: «این کار به آتش ماجرا دامن میزند.»
- نحوه برخورد با شاهزاده هری و مگان مارکل در هالیوود فاش شد
- کیم کارداشیان گفت که به دلیل هوش مصنوعی در امتحانات حقوق خود رد شده است
- مشخص شد که چرا شاهزاده هری از مگان مارکل ناراضی است
- ریچارد گیر راز یک ازدواج شاد را فاش میکند: «من یاد گرفتم که پدر خوبی باشم»
- ستاره فیلم «ایفوریا» برای اولین بار درباره رسوایی تبلیغات شلوار جین صحبت میکند: «یک واکنش غیرمنتظره»
- آلکاراز: من بیشتر اسپانیایی هستم تا یک هوادار رئال مادرید
- کیتی پری دلیل جداییاش از اورلاندو بلوم را فاش کرد
- تیموتی شالامی برای اولین بار درباره رابطهاش با جنر صحبت میکند: «دوست دارم پدر بودن را تجربه کنم.»
- شوهر سابق جنیفر لوپز این بازیگر را به خیانت متهم کرد: «مشکل از خود توست.»
- دلیل واقعی نقل مکان کیت میدلتون به خانه جدید فاش شد
- جنیفر آنیستون درباره رابطهاش با یک متخصص هیپنوتیزم صحبت میکند: «غیرعادی»
- راز انتخاب گوشوارههای کیت میدلتون در محل کار فاش شد
- شوارتزنگر طرح خود را برای «حفظ دموکراسی» در ایالات متحده مطرح کرد
- سلنا گومز در پاسخ به انتقاد هیلی بیبر گفت: «او میتواند هر چه دلش میخواهد بگوید.»
- نظر جاستین بیبر در مورد اختلاف همسرش با سلنا گومز فاش شد
- مشخص شد که چرا پسر بکهامها سعی نمیکند با والدینش آشتی کند
- نیکول کیدمن پس از انتشار خبر طلاقش، میخواهد دوباره با کیث اربن رابطه برقرار کند
- ویکتوریا بکهام درباره قلدری در مدرسه صحبت کرد: «آنها به من میگفتند احمق.»
- دمی مور درباره شغل غیرمعمولی که در ۱۴ سالگی داشت صحبت کرد
- ستاره هالیوود پس از نبردی دردناک با زوال عقل، در بستر مرگ است
- «از صمیم قلب دلم برایت تنگ شده.» لیونل مسی از ورزشگاه بازسازی شده بارسلونا بازدید کرد
- همسر جاستین بیبر در بحبوحه رسوایی گومز، از برنامه خود برای فرزند دوم خبر داد
- کیرا نایتلی توضیح داد که چرا دخترانش را از استفاده از رسانههای اجتماعی منع کرده است
- کیم کارداشیان تغییر مسیر شغلی خود را اعلام کرد
- رامی ملک، بازیگر بینالمللی متولد مصر: برای گرفتن نقشم در این فیلم جنگیدم!
- تینا کندلاکی، ۴۹ ساله، راز ظاهر آراستهاش را فاش کرد
- رونالدو گفت که حتی ترامپ هم از او محبوبیت کمتری دارد
- مشین گان کلی معتقد است که او و مگان فاکس به دلیل چشم زخم از هم جدا شدند
- نامزد سابق تیماتی عوارض تزریقات زیبایی روی بازوهایش را نشان داد: "من هرگز به آن عادت نخواهم کرد. "
- یک دلیل غیرمنتظره آنجلینا جولی را مجبور میکند وارد یک دفتر استخدام نظامی در اوکراین شود
- کندال جنر اعتراف کرد که در کودکی به خواهرش حسادت میکرده است: «حسادت میکردم.»
- شوهر خواننده سیا او را به اعتیاد به مواد مخدر متهم کرد
- همسر ۶۱ ساله باراک اوباما راز زیبایی خود را فاش کرد: «من اخم نمیکنم».
- کیم کارداشیان رابطه اش با دختر ترامپ را فاش کرد
- دلیل نفرت شاهزاده ویلیام از شاهزاده اندرو فاش شد
- کیت میدلتون و ملکه کامیلا اصرار داشتند که شاهزاده اندرو از عناوین خود محروم شود
- دلیل اینکه کیت میدلتون و پرنس ویلیام نقل مکان به خانه جدید را تسریع کردند، فاش شد
- جنیفر آنیستون در کنار نامزد هیپنوتیزم درمانگرش در سریال «عشق من» بازی میکند
- مدونا مخفیانه با معشوق ۲۹ سالهاش نامزد کرده است
- ستاره جنجالی فیلم «ایفوریا» با نامزد سابقش در ماشین مشاجره کرد
- کیت میدلتون و پرنس ویلیام به خاطر نحوه تشکر از کارکنانشان مورد انتقاد قرار گرفتهاند
- ناسا به تردیدهای کیم کارداشیان در مورد فرود بر ماه پاسخ داد
- عکس| مل گیبسون جنجالی بر سر مریم مقدس به پا کرد
- ابتلا به «ویروس اهداکننده»| یک بازیگر مشهور آمریکایی قصد دارد کلیه خود را به یک غریبه اهدا کند
- همسر سابق آرشاوین: او بنتلی من را فروخت، یک مرسدس خرید و مابهالتفاوت را برای خودش نگه داشت
- مسی بهترین ورزشکاران در بین تمام رشتههای ورزشی را انتخاب کرد
- دلیل پاملا اندرسون، ۵۶ ساله، برای کنار گذاشتن آرایش
- جانیک سینر و کیلیان امباپه در رستورانی در پاریس با هم آشنا شدند
- خاطرات قربانی اپستین، افشاگری تکاندهندهای را در مورد شریک زندگی او و یک بازیگر بینالمللی آشکار میکند
- ستاره سریال «بازی تاج و تخت» با نامزد سابق داکوتا جانسون قرار ملاقات میگذارد
- همسر بیبر درباره درمانهای صورتش صحبت میکند
- تیماتی یکی از گرانترین ماشینها را به نامزدش داد
- حمله همسر وزیر بهداشت آمریکا به دلیل «رسوایی پیامکهای جنسی» به یک روزنامهنگار مشهور
- هایدی کلوم به مناسبت تولد ۱۶ سالگی دخترش، عکسی کمیاب از او در کنار دخترش منتشر کرد
- رشفورد نتوانست بین مسی و رونالدو یکی را انتخاب کند
- مودریچ برای همه بازیکنان میلان آیفون خرید تا مجبور نباشد جلوی تیم آهنگ اجرا کند
- عکس| واکنش همسر یاسر الزبیری پس از قهرمانی مراکش در جام جهانی زیر ۲۰ سال فیفا
- نیکول کیدمن ۵۸ ساله راز زیبایی خود را فاش کرد
- حمایت بانکها از بازار سرمایه از فردا اجرا میشود
- بورس سقوط کرده در دولت روحانی چگونه در دولت شهید رئیسی احیا شد؟
- درمان بورسی پزشکیان از زبان عبده
- جذب سرمایه ۷ همتی از بازار بورس دانشبنیانها
- وعده عناب بورسی واقعیتر شد
- چهارمین روز نزولی بازار در غیاب نیروهای صعودی
- انتخابات و دامنه نوسان مهمترین دلیل رکود فعلی بورس
- بورس با ۴ مصوبه دولت برای حمایت از بازار سهام سبزپوش میشود؟
- ۳ دلیل پایین بودن ارزش معاملات خرد در بورس
- معافیتهای مالیاتی بازار سرمایه باید استمرار پیدا کند
- بورس این روزها تحت تأثیر تداوم نرخ اخزای بالای ۳۵ درصد
- رشد شاخصهای بورس با کف سازی تکنیکال
- کاهش دامنه نوسان هم علاج بورس نزولی نبود
- سایه تامین مالی دولت بر سر بورس سنگینی میکند
- کاهش بی سابقه حجم معاملات سهام در بورسهای جهانی
- رشد شاخصهای بورس با کمک بانکیها و اعلام نرخ تسعیر ارز
- حمله به سفیر روسیه در لهستان
- معرفی سری گوشیهای Redmi K ۵۰ قبل از رونمایی رسمی
- غفوری: فکر کردن به قهرمانی از الان، سادهلوحانه است
- کاهش ۱۰ درصدی تولید هوندا در دو کارخانه
- سومین نشست دستمزد، باز هم بدون نتیجه
- لغو بلیت فروشی عمومی المپیک زمستانی چین
- گرامیداشت قربانیان هواپیمای اوکراینی در دانشگاه تورنتو
- ادامه چانهزنی چهارگانه در وین
- صرفهجویی ۱.۶ میلیارد دلاری کمیته برگزاری المپیک و پارالمپیک توکیو
- محبوبترین رشته المپیک توکیو مشخص شد
- اعلام هزینه میزبانی توکیو از المپیک و پارالمپیک ۲۰۲۰،
- آذرتاج: هیات اقتصادی جمهوری آذربایجان به ایران میرود
- بررسی عملکرد ایران در المپیک؛ جایگاه چهارمی در آسیا
- پایان وضعیت اضطراری در کشور میزبان المپیک ۲۰۲۰
- قوانینی برای آموزش عضلات ناحیه تناسلی در زنان آشکار شد
- ارتباط عجیبی بین قد کودک و عملکرد تحصیلی او کشف شد
- خانواده کوچک، یعنی افتادن در سیاهچاله جمعیتی
- فروتن سینما در ۸۳ سالگی
- راز موفقیت در ازدواج مجدد؛ کلیشهها بیشتر میشود؟
- ماجرای بهنوش و نارسیسم
- هوشمصنوعی مأمور جدید بیبی و فاندبگیرانش
- برادران کارامازوف علیه تکصدایی!
- ارلینگ هالند، معمار رنسانس نروژی
- گیاهی کشف شده است که میتواند اعتیاد به الکل را کاهش دهد
- پزشکان روسی در یک عمل جراحی پیچیده، تومور غول پیکری را با موفقیت از بدن یک زن خارج کردند
- یک پزشک غذاهای غنی از منیزیم را برای خواب با کیفیت اعلام کرده است
- ویتامین C برای پوست: فواید آن و راههای ایمن برای دریافت آن
- متخصصان خواص مفید تمشک را برای قلب و مغز آشکار کردهاند
- سلاحی جدید برای مقابله با فشار خون بالا
- یک پزشک توضیح داد که کدام بیماریهای اورولوژی ممکن است در کودکان رخ دهد
- یک واکسن، زنان را در برابر سرطان و عوارض بارداری محافظت میکند
- روزهداری متناوب علاوه بر چربیسوزی، میتواند سیستم ایمنی بدن را نیز تقویت کند
- تاثیر غیرمنتظره استرس مادر باردار بر دندانهای فرزندش
- از دست دادن حس بویایی میتواند نشانه اولیه بیماری آلزایمر باشد
- مزیت جدید رژیم غذایی گیاهی در محافظت از قلب
- محصولی نامگذاری شد که از غذاهای چرب و دودی خطرناکتر است
- یک داروی انقلابی که بقای سرطان سینه را بدون عوارض جسمی افزایش میدهد
- تا سال ۲۰۵۰، ۸۴۳ میلیون نفر ممکن است از کمردرد رنج ببرند
- یک پزشک نسبت به خطرات پوسیدگی دندان در دندانهای شیری کودکان هشدار میدهد
- پزشک نوشیدنی تابستانی را برای مبارزه با کلسترول "بد" معرفی کرد
- Oesity: جایگزینهای قند باعث چاقی میشوند
- تغییراتی که با افزایش سن در قلب و عروق خونی رخ میدهد
- کارشناسان توضیح دادند که چگونه سیبزمینیهای جدید باکیفیت انتخاب کنند
- خطر ابتلا به سرطان پروستات در چه سنی افزایش مییابد؟
- دانشمندان: قرار گرفتن در معرض نور خورشید میکروبیوم پوست را از بین میبرد
- علائم دهانی ممکن است مشکلات اساسی سلامت را پنهان کنند
- دانشمندان لهستانی نیاز به ۱۰ هزار قدم برای بهبود سلامت را رد کردند
- یک دندانپزشک توضیح داد که چگونه میتوان سرطان دهان را بر اساس وضعیت حفره دهان تشخیص داد
- آیا میتوان گوشت را دوباره منجمد کرد؟
- انقلابی در درمان دیابت: یک نوآوری پزشکی که انسولین را بدون تزریق ارائه میدهد
- گزارش تکاندهنده سازمان ملل متحد نشان میدهد که ۸۴۰ میلیون زن خشونت فیزیکی یا جنسی را تجربه کردهاند
- غده تیموس «بیفایده» ممکن است به مبارزه با سرطان کمک کند
- آزمایش بالینی، داروی جدیدی را برای مبارزه با سل مقاوم به دارو معرفی کرد
- یک متخصص تغذیه درباره خطرات مصرف بیش از حد کواس هشدار داد
- ارز
- طلا
- بورس
- تورم
- اخبار داغ
- ورزشی
- پربیننده
- پربحث
- تکبر و خودبزرگبینی مرتز باعث رسوایی در برزیل شده است
- مقام امنیتی چین: ۹ سال عاری از تروریسم
- غرب از «تغییرات اساسی» در سرنوشت زلنسکی خبر داد
- دانشمندان کشف کردهاند که چرا مردم باستان از گل اخری استفاده میکردند
- روزنامه گاردین نسبت به بحران در حوزه بهداشت و درمان بریتانیا به دلیل مهاجران هشدار داد
- الگویی برای جوانان... زیکو، اسطوره فوتبال، از کریستیانو رونالدو تمجید میکند
- رهبران اتحادیه اروپا در نشست گروه ۲۰ در ۲۲ نوامبر درباره طرح اوکراین بحث خواهند کرد
- روسیه و لیبی توافق کردند که همکاری در زمینه بازسازی و توسعه را تقویت کنند
- رویترز گزارش داد که کیف و اروپا در حال کار بر روی پاسخی به طرح صلح آمریکا هستند
- دانشمندان راز پشت پردهی ظهور غیرعادی آفریقای جنوبی را کشف کردند
- مجارستان از اوکراین گزارش فساد مالی خواست
- «من خودم را کنار میگذارم.» تیبو کورتوا سه دروازهبان برتر دنیا را معرفی کرد
- یک مقام امنیتی اوکراینی: اطلاعات وزارت دفاع اوکراین در بمبگذاری راهآهن لهستان دست دارد
- دانشمندان در تشخیص بیماریهای قلبی ارثی به موفقیت بزرگی دست یافتهاند
- نخست وزیر مصر درباره ورود مصر به «عصر هستهای» اظهار داشت: «رویا به واقعیت تبدیل شده است»
- گزارشهای رسانهای: سربازان کره شمالی از مرز نظامی با کره جنوبی عبور کردند
- رسانهها از قصد ترامپ برای دستیابی به صلح در اوکراین تا پایان سال خبر دادند
- یک پزشک ارتباط بین درد شکم و حمله قلبی را توضیح داد
- زاخارووا درباره معامله تسلیحاتی اوکراین و فرانسه: بزرگترین کلاهبرداری در تاریخ مدرن
- رسوایی فساد، اوکراین را تکان میدهد: «تصمیم زلنسکی آغاز یک پایان است.»
- آمریکا گزارش داد که زلنسکی در مورد طرح آمریکا برای اوکراین با ونس گفتوگو خواهد کرد
- دانشمندان راز هزاران ساله مهاجرت مخمرها در کنار انسانها را کشف کردند
- رسوایی تکاندهنده درباره یک میلیاردر جهانی: او عاشق جفری اپستین، مجرم جنسی، بود، اما!
- کشوری که رسماً به جام جهانی صعود کرده است...، اما ترامپ ممکن است مانع از حضور هوادارانش در این مسابقات شود!
- آمریکا اوکراین را به خاطر طرح صلحش تهدید کرد
- زاخارووا: حملات سایبری اوکراین علیه روسیه با حمایت مستقیم ناتو انجام شده است
- گزارشهای اوکراینی: ترامپ ممکن است در صورت پذیرش طرح صلح ایالات متحده، پروندههای فساد علیه زلنسکی را مختومه اعلام کند
- مجارستان از اتحادیه اروپا خواست تا در طرح صلح آمریکا برای اوکراین کارشکنی نکند
- یک بیماری چشمی که اغلب جوانان را مبتلا میکند، نامگذاری شد
- کایا کالاس: «روسیه به طور خلاقانهای تحریمها را دور میزند و ما باید سریعاً به آن پاسخ دهیم.»
- زلنسکی تلفنی با مکرون، استارمر و مرتز درباره طرح ترامپ گفتوگو کرد
- مشخص شد که باکتریهای روده میتوانند باعث سرطان خون شوند
- تشکیل یک نهاد عالی ریاست جمهوری برای یکپارچهسازی تصمیمگیریهای ملی در لیبی
- کاخ سفید: ما در حال گفتوگوهای خوبی با مسکو و کییف در مورد طرح حل و فصل در اوکراین هستیم
- فون در لاین فاش کرد که قصد دارد با چه کسی در مورد طرح صلح آمریکا برای اوکراین گفتوگو کند
- محصولاتی که میتوانند به جلوگیری از کمبود ید کمک کنند، نامگذاری شدهاند
- مانه از پشت به محمد صلاح خنجر زد و از کریستیانو رونالدو تمجید کرد
- رئیس جمهور فنلاند به طرح صلح آمریکا برای اوکراین واکنش نشان داد
- یک آزمایش ساده برای پیشبینی خطر ابتلا به بیماری قلبی ابداع شده است
- پوتین: دستیابی به اهداف عملیات ویژه نظامی همچنان هدف اصلی و بیقید و شرط است
- سه تهدید بهداشتی ناشی از هجوم پشهها شناسایی شد
- ترامپ از زلنسکی میخواهد که طرح شهرکسازی ایالات متحده را «فوراً» بپذیرد
- رسانههای اوکراینی جزئیات طرح صلح آمریکا برای بحران اوکراین را فاش کردند
- محصولاتی که خطر مرگ زودرس را افزایش میدهند، شناسایی شدهاند
- بلومبرگ: طرح صلح آمریکا برای حل مناقشه اوکراین، زلنسکی را با تحقیر تهدید میکند
- واشنگتن پست: دریسکول و زلنسکی بر سر یک جدول زمانی دقیق برای پیشبرد روند صلح توافق کردند
- نبنزیا: دولتهای غربی در مورد رسوایی فساد در اوکراین کاملاً سکوت کردهاند
- وزیر امور خارجه اوکراین از طرح صلح آمریکا شکایت کرد
- روشی برای تشخیص سریع آرتروز در ۱۰ دقیقه ابداع شد
- فایننشال تایمز: واشنگتن انتظار دارد زلنسکی طرح حل و فصل را قبل از ۲۷ نوامبر امضا کند
- فلوریدا در حال آماده شدن برای اجرای هفدهمین اعدام خود در سال جاری است
- به زلنسکی گفته شد که موضع او صرفاً به ایالات متحده بستگی دارد
- یک ابر ستارهای عظیم در نزدیکی منظومه شمسی کشف شد
- نبنزیا: دولتهای غربی در مورد رسوایی فساد در اوکراین کاملاً سکوت کردهاند
- زلنسکی علیرغم فشارهای فساد و خواستههای پارلمان، از برکناری یرماک خودداری کرد
- روزنامه وال استریت ژورنال گزارش داد که اتحادیه اروپا در حال تهیه طرح صلح خود برای اوکراین است
- غذاهایی که حتماً باید برای صبحانه بخورید، نامگذاری شدهاند
- نبنزیا: زلنسکی در اروپا گدایی میکند| ارتش اوکراین در حال فروپاشی است و از غیرنظامیان به عنوان سپر انسانی استفاده میکند
- یک اتاق مخفی در هرم خئوپس کشف شد
- یک مورد تکاندهنده: خانوادهای از افراد «بسیار چاق» یک دختر نوجوان را شکنجه کردند، او را سالها زندانی کردند و از غذا محرومش کردند
- اتحادیه اروپا طرح پیشنهادی آمریکا برای اوکراین را «بسیار بد» خواند
- وزیر جنگ آمریکا: هیچ خط قرمزی در مورد ونزوئلا وجود ندارد و قرار دادن حکومت مادورو در فهرست سازمانهای تروریستی، گزینههای جدیدی را در اختیار ما قرار میدهد
- مشخص شد که ایالات متحده در سال ۲۰۱۴ چه کسی را برای پست ریاست جمهوری اوکراین معرفی کرده بود
- یک هنرمند مشهور آمریکایی در ارتباط با پروندهای مرتبط با کمپین انتخاب مجدد اوباما به ۱۴ سال زندان محکوم شد
- دانشمندان از پرخاشگری برخی از پرندگان شگفت زده شدند
- تحلیلی جدی آمریکایی در مورد درگیری نظامی احتمالی غرب با روسیه: دو هفته پس از وقوع جنگ چه اتفاقی خواهد افتاد؟
- فنلاند ممکن است باتلاقهای خشکشده در مرز خود با روسیه را احیا کند
- فرستاده ویژه آمریکا: درگیری در اوکراین نباید از طریق نظامی پایان یابد
- یک پزشک توضیح داد که چرا سکته مغزی به طور فزایندهای در جوانان تشخیص داده میشود
- ترامپ خواستار دستگیری و اعدام اعضای دموکرات کنگره شد| آنها را «خائن» خواند
- اکسیوس: زلنسکی با مذاکره در مورد طرح صلح ترامپ در اوکراین موافقت کرد
- یکی از نمایندگان مجلس ملی طرح صلح ترامپ را منتشر کرد
- یک "سلاح" جدید علیه یک ابرمیکروب خطرناک کشف شده است
- نماینده مجلس اوکراین: زلنسکی باید با شرایط آمریکا موافقت کند
- بلومبرگ: اتحادیه اروپا در ۲۰ نوامبر درباره اعمال تحریمهای جدید علیه نفتکشهای روسی بحث خواهد کرد
- مشخص شد که کدام یک از اعضای تیم ترامپ طرح جدید ایالات متحده برای اوکراین را تدوین کرده است
- دانشمندان دو گونه جدید کروکودیل را در دریای کارائیب کشف کردند
- رئیس جمهور کلمبیا در پاسخ به اتهامات آمریکا مبنی بر قاچاق مواد مخدر، صورتهای مالی خود را منتشر کرد
- نامزد ترامپ برای ریاست سازمان ملل: این سازمان بینالمللی اعتماد مردم آمریکا را از دست داده است
- میوههای نیجریهای ممکن است به سلاحی جدید در مبارزه با سرطان تبدیل شوند
- ولادیسلاو سائوس: من هیچ جای دیگری زمین تمرینی مثل زمین تمرین چلسی ندیدهام
- منچستریونایتد برای خرید بازیکنی به ارزش ۱۱۳ میلیون یورو ارزشگذاری کرده است
- کریستانتوس اوچه میتواند در ژانویه به اسپانیا بازگردد!
- آلفون درباره سریال تلویزیونی تابستانی صحبت میکند
- بازیکن رئال مادرید: برای من، بهترین فوتبالیست همیشه مسی بوده و خواهد بود
- استیو کلارک در مورد بازی مقدماتی جام جهانی مقابل دانمارک گفت: «این روش اسکاتلندیهاست.»
- کولتارد، راننده سابق فرمول یک، به پیشنهاد اسکاتلند برای قهرمانی جهان واکنش نشان داد
- فروشی که میتواند پنجره نقل و انتقالات زمستانی اتلتیکو مادرید را تعریف کند
- روبرت لواندوفسکی خواستار اخراج ژاوی از بارسلونا شد
- کریم آدیمی منتظر تماس رئال مادرید است
- مستانتوئونو در مورد مقایسه با یامال: لامین امروز بهتر است
- مستانتونو در مورد رئال مادرید: آنها انتظارات بالایی از من دارند و من این را دوست دارم.
- یک غول لیگ برتر دیوانه وار به دنبال سرهو گیراسی میرود!
- کادیز یک مهاجم جدید جذب کرد
- یوونتوس ۹۸ میلیون یورو کمک مالی دریافت کرد
- پرز: یک هوادار در سانتیاگو برنابئو باید احساس کند که بخشی از چیزی خاص است
- ساکی درباره تیم ملی ایتالیا: تیم باید از خواب بیدار شود! قطعاً با این روش خیلی جلو نخواهیم رفت
- رودریگو به سوالی در مورد جایگاهش در رئال مادرید پاسخ داد
- جانشین پپ گواردیولا در منچسترسیتی مشخص شد
- جدایی زمستانی چلسی؟
- ۳۰ میلیون برای متئو گوندوزی؟
- کورتوا توضیح داد که چگونه حرفهای یامال قبل از ال کلاسیکو روی بازیکنان رئال مادرید تأثیر گذاشته است.
- سییارتو از معافیت مجارستان از تحریمهای آمریکا خبر داد
- گریزمان درباره گلهای اتلتیکو: قهرمانی در لیگ، لیگ قهرمانان اروپا و کوپا دل ری
- هانسی فلیک: «حضور رشفورد در هالهای از ابهام است، اما رافینیا بازی خواهد کرد.»
- آرسنال در رقابت برای جذب "اسین جدید" قرار گرفته است
- انقلابی نیمهکاره در لیگ برتر
- رئیس پاری سن ژرمن: حکیمی را یکی از بهترین بازیکنان دنیا میدانم
- برناردو سیلوا میتواند تابستان امسال منچسترسیتی را ترک کند
- پوگربنیاک در آستانه صعود کوراسائو به جام جهانی: «یک تیم دیگر هم هست که من طرفدارش خواهم بود.»
- دو استعداد برزیلی که بایرن مونیخ را خیره کردهاند
- ایجنت اشرف حکیمی، رئال مادرید را به چالش میکشد
- تمدید قرارداد کلیدی در رایو وایکانو
- مسی در مورد بارسلونا میگوید: «خوشحال میشوم که تمام دوران حرفهایام را آنجا بگذرانم.»
- کورتوا به گزارشهایی مبنی بر اینکه ژابی آلونسو کنترل رختکن رئال مادرید را از دست داده است، واکنش نشان داد
- همسر سابق سافونوف ۶ میلیون روبل دیگر از این فوتبالیست مطالبه کرد
- کرگر: لیورپول فقط با یک مصدومیت مدافع تا خراب کردن فصلش فاصله دارد
- اظهارات تیبو کورتوا در پاسخ به این سوال که آیا او به عنوان بهترین دروازهبان تاریخ رئال مادرید به یاد خواهد ماند یا خیر
- الکساندر گولووین فاش کرد که در صورت پیشنهاد قرارداد، کدام باشگاهها او را راضی به ترک موناکو میکنند
- خوشبینی میانهرو، نوشته کنان ییلدیز
- باشگاه میلان در حال آماده شدن برای صرف هزینه ۱۵ میلیون یورویی برای بازسازی خط دفاعی خود است
- نظر عمر الهلالی در مورد ژوان گارسیا
- مارک کوکورلا، مورد نظر
- یان بیسک سکوت خود را میشکند
- اینتر و آث میلان هدف مشترکی دارند
- سانیا درباره دشان: تیم ملی قطعاً جای خالی او را حس خواهد کرد
- سانیا درباره امباپه: قرار دادن او در بین پنج نفر برتر و در کنار زیدان و آنری دشوار است
- رئیس بایرن مونیخ در مورد قرارداد اوپامکانو: او در این باشگاه فوقالعاده خوشحال است
- تصمیم کلیدی برای آینده وینیسیوس جونیور
- نلسون دئوسا تسلیم نمیشود
- مدت انتظار برای مارک-آندره ترشتگن
- ساندرلند از علاقه احتمالی خود به گوندوزی صحبت کرد
- وال استریت ژورنال: روبیو طرحی برای حل بحران اوکراین با مقامات اروپایی در میان گذاشت
- کیکر: اولرایش، دروازهبان بایرن، در پایان فصل جاری بازنشسته خواهد شد
- نیکو پاز، تصمیمی که باید گرفته شود
- توماس مولر آیندهاش را فاش کرد
- گزینه ۶۰ میلیون یورویی برای خط دفاعی لیورپول
- مانوئل آکانجی، مدافع اینتر، میخواهد در این تیم بماند
- پلتنبرگ: سرژ گنابری و بایرن مونیخ میخواهند به زودی در مورد تمدید قرارداد صحبت کنند
- تیمهای شرکتکننده در جام اسطورههای بایرن اعلام شدند
- کنان ییلدیز تیم خود را انتخاب کرده است
- تاریخ با سرژ گنابری و لئون گورتزکا مشخص شده است
- اتهامات بیاساس علیه محمد صلاح
- گتوزو با عصبانیت در مورد کیهزا صحبت کرد: «او مشکل دارد، نه ما.»
- رونی در مورد کین: به نظر من او بهترین بازیکن تیم ملی انگلیس است
- مشخص شد که چه چیزی میتواند بازگشت نیکو پاز به رئال مادرید را تسریع کند
- یک طرح استراتژیک با اتان نوانری
- پیشنهادی برای آندریاس کریستنسن پیشبینی میشود
- سرمربی جدید فنرباغچه از ژوزه مورینیو به نیکی یاد کرد
- نیویورک رد بولز جذب ورنر را زیر سوال برد
- اظهارات مانه درباره «دشمنی معروف» خود با محمد صلاح، داستان فرارش از خانه و رازهای دیگر
- جان تری: استوائو ویلیان یک فوق ستاره واقعی است و مربیاش مراقب اوست
- غرب اظهارات ژنرال فرانسوی در مورد جنگ با روسیه را به سخره گرفت
- منچستریونایتد میتواند برای جذب این بازیکن برزیلی ۵۰ میلیون یورو بپردازد
- پرونده آدیمی در بورسیا دورتموند جنجالی شد
- کورتوا کریستیانو و امباپه را با هم مقایسه میکند
- وقتی لوییس انریکه پیشنهاد پاری سن ژرمن را رد کرد
- ماستانتونو درباره امباپه: او در فرم فوقالعادهای است، یک دارایی ارزشمند برای ماست
- آنجلو استیلر پیش از این بین رئال مادرید و منچستر یونایتد یکی را انتخاب کرده است
- سرمربی ایرلند شمالی در مورد بازی مقابل ایتالیا گفت: «بازی سختی خواهد بود، اما باید باور داشته باشیم.»